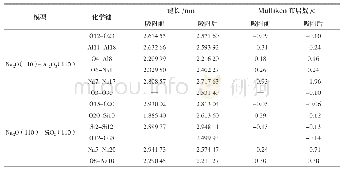
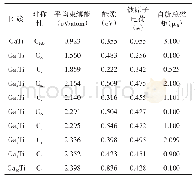
《表1 B6Li2·nH2团簇Li-B、H2-Li、H-H的平均键长和平均吸附能以及自然电荷分布》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《Li原子修饰一维六角硼烯链团簇的结构及储氢性能研究》
研究H2在Li修饰的一维六角硼烯链团簇表面的吸附,采取在每个Li周围分别吸附从一个到多个H2的方式依次添加,利用B3LYP/6-311++G(d,p)方法进行结构优化和频率计算,最终得到稳定结构(B6Li2.nH2)m,结构分别显示为B6Li2.nH2(如图5)和(B6Li2.nH2)2(如图6)。H2在Li修饰一维单孔六角硼烯团簇表面吸附的结构特征列于表1。由图5a—5d可见,随着吸附H2的数目增大,B6Li2结构基本未发生变化,其B-B平均键长仍为1.549?,Li-B平均键长随吸附H2的数目增大稍有增大,变化范围为2.319~2.334?,表明B6Li2结构具有较好的稳定性,可作为稳定的基底用于吸附储氢。Li与H2平均距离随吸附H2的数目增大而增大,结合H2在B6Li2团簇表面吸附的平均吸附能,表明H2与B6Li2团簇的相互作用在逐渐减弱,平均吸附能数值表明H2可以介于物理吸附和化学吸附之间的方式与B6Li2团簇结合。由图5c可见,6个H2吸附时,每个锂原子周围均可吸附三个H2不发生远离,但当8个H2吸附时(图5d),则出现H2与Li间距突然增大的情况,表1可见此时H2的平均吸附能变得很小,逐渐转变为纯粹的物理吸附,故认为6个H2(每个锂原子有效吸附三个H2)可以稳定吸附在单孔B6Li2团簇表面。
| 图表编号 | XD00162298500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.03.01 |
| 作者 | 吴永波、甘雅玲、陈施婷、陈银坤、阮文 |
| 绘制单位 | 井冈山大学数理学院、井冈山大学数理学院、井冈山大学数理学院、井冈山大学数理学院、井冈山大学数理学院 |
| 更多格式 | 高清、无水印(增值服务) |