《表6 在M06-2X/6-311G(d,p)水平下计算得到的[HEtHex][Acylala]的氢键BCP的电子密度性质》
![《表6 在M06-2X/6-311G(d,p)水平下计算得到的[HEtHex][Acylala]的氢键BCP的电子密度性质》](http://bookimg.mtoou.info/tubiao/gif/HGSZ2020S1003_03200.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《异辛基乙二胺-酰基丙氨酸型质子化离子液体的分子间氢键相互作用》
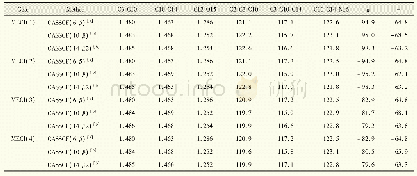
Bader的AIM理论在计算化学中被广泛使用,AIM理论能够精确地判断化学键的相互作用的强度和性质[28]。本研究利用AIM理论对阴阳离子对的氢键临界点(bond critical point,BCP)处的电子特性进行了理论分析。表6列出BCPs处的电荷密度(ρc)、Laplace值(?2ρc)以及氢键能(EHB),其中ρc用来表示原子间成键的强弱,ρc越大,表明该处的氢键作用越强,反之氢键作用越弱。在一定范围内氢键的强弱与ρc的大小呈正相关。一般而言,ρc值在共价键中大于0.20 a.u.,在氢键相互作用中小于0.10 a.u.。[HEtHex][Butlala]及[HEtHex][Hexlala]所有构型中的ρc值在0.061~0.076 a.u.范围内,均小于0.10 a.u.,说明[HEtHex][Acylala]分子间具有较强的O—H…N型氢键。Laplace值?2ρc是ρc的二阶导数,可以判断原子成键的类型。当?2ρc<0,则表明BCP处的电荷是积聚的,相邻的两原子之间以共价键形式存在;相反,如果?2ρc>0,表明BCP处的电荷是发散的,相邻的两个原子之间以氢键、离子键等闭壳层作用存在。[HEtHex][Butlala]及[HEtHex][Hexlala]的EHB分别在18.69~24.19 kcal?mol-1和18.72~23.95 kcal?mol-1范围内,且EHB大小趋势均为S5>S4>S2>S1≈S3,即[HEtHex]2+构型的氢键能比[HEtHex]1+构型强。当阳离子均为异辛基乙二胺,阴离子碳链由丁基增长至己基时,氢键能没有明显的变化,如[HEtHex][Butala]S5(24.19 kcal?mol-1)≈[HEtHex][Butala]S5(23.95 kcal?mol-1);[HEtHex][Butala]S1(18.76 kcal?mol-1)≈[HEtHex][Butala]S5(18.72 kcal?mol-1)。
| 图表编号 | XD00159134900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.04.01 |
| 作者 | 刘佳鑫、徐宇、花儿 |
| 绘制单位 | 北方民族大学化学与化学工程学院、北方民族大学化学与化学工程学院、北方民族大学化学与化学工程学院、北方民族大学国家民委化工技术基础重点实验室、北方民族大学宁夏太阳能化学转化技术重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |
![表5[HAlkyl][TFSA]的主要氢键作用部位BCP处的电子云密度特征](http://bookimg.mtoou.info/tubiao/gif/SHZN202005004_04900.gif)
![表7 文献值中较强氢键的指标[29-30]及本研究中[HEtHex][Acylala]分子间氢键的特征值](http://bookimg.mtoou.info/tubiao/gif/HGSZ2020S1003_03300.gif)