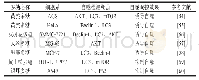
《表1 ASD风险基因参与自噬调控机制》
自噬通过清除神经元中异常聚集的蛋白质、缺陷细胞器和异常膜结构等维持神经元存活和稳态,选择性靶向突触小泡等突触成分调节突触可塑性和社交缺陷等ASD样行为表型。ASD风险基因能参与调控自噬(表1),且自噬相关基因及调节因子m TOR、PI3K、AKT、ULK1、Beclin-1和ATG7等均参与调节ASD发病机制。在FXS中,上调的m TOR与突触功能和行为异常相关,且PI3K-AKT-m TOR信号失调与FXS小鼠的树突棘形态异常和学习记忆障碍相关,提示抑制相关信号通路来激活自噬有望成为改善突触和认知功能异常的新途径;在TSC中,自噬缺陷、m TOR过度活化与TSC小鼠社交和认知功能障碍密切相关;在RTT中,Me CP2基因突变导致自噬失调和AKT-m TOR等相关信号分子异常进而破坏大脑功能,从而产生ASD相关病理表型和自闭症样行为。在ASD模型鼠中使用雷帕霉素(自噬激活剂)能改善突触可塑性和行为缺陷等认知功能障碍。深入研究自噬调节ASD的信号转导途径和分子机制,以及在ASD发展过程中的动态变化,才能更加完整地阐明ASD中自噬途径发挥的重要作用,使调节自噬成为防治ASD药物研究的新途径。
| 图表编号 | XD00154471700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.08.01 |
| 作者 | 张思铭、陈雨珊 |
| 绘制单位 | 武汉科技大学医学院脑科学先进技术研究院、武汉科技大学医学院脑科学先进技术研究院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式