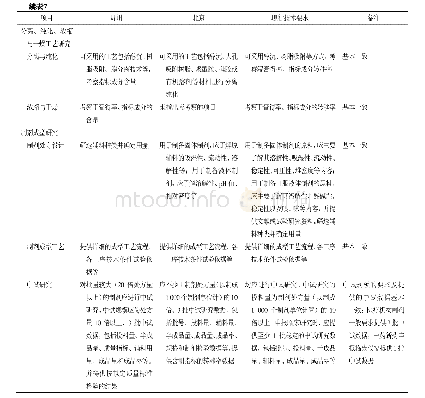
《表1 不同版本对比表:医疗器械说明书的控制要求》
*为不涉及生产企业机密,警示条款具体内容予以省略
现场核查该公司盖有“受控文件”专用章的说明书,其版本号为2016-1版,于2016年11月1日批准,其中安全警示事项共10条,注意事项共5条;比2014-1版说明书增加了2条警示事项、1条注意事项(表1)。其内容有明显差异,属于潜在的安全危害、使用限制内容及与其他医疗器械联合使用的注意事项等重要信息不一致。经核查企业已提交注册变更申请的说明书文本中,其安全警示事项中也未涵盖该受控版本的第9条内容。工作人员陈述:该变更此前已提交有关审批部门但未得到书面批复、回执,故按照规定“在20个工作日内未收到批复”则视为已同意申请的变更事项。
| 图表编号 | XD00141974200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.03.28 |
| 作者 | 李宝林、李博诚、张发勇 |
| 绘制单位 | 河北省医疗器械与药品包装材料检验研究院、吉林大学公共卫生学院医学信息学系信息检索教研室、河北省医疗器械与药品包装材料检验研究院物理室 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式