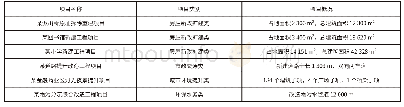
《表1 药品在不同环节存在安全问题的表现及具体案例》
资料来源:作者根据资料整理得到。
药品研发是药品质量安全的源头,就好像基因决定癌症患者的状况一样,一旦源头出现问题,最终在消费者使用时肯定会存在药品安全风险。药品研发环节存在的安全问题主要包括:一是药品研发过程中对药品未知的不良反应未充分进行挖掘及预测,导致药物的不良反应(具体案例见表1,下同)。2018年国家药品监督管理总局发布的药品不良反应监测报告中指出,2017年我国有98%的区县报告了药品不良反应,较2016年有所增长。另外,根据我国安全注射联盟的统计数据显示,每年有近20万人死于药物不良反应。二是药品的临床试验数据记录不规范,对原始数据没有保存和备份,甚至弄虚作假。2015年7月国家食品药品监督管理总局(以下简称“国家食药总局”)对待批生产的1622个药物临床试验项目进行核查时发现,约八成数据不真实、不完整、不规范,11家药品研究机构被立案调查(1)。另据国家食药总局统计,2017年全国收回药品GMP证书157张,发回药品GMP证书64张。三是临床研究样品的制备规模小,试制条件和质量与批量生产时相比差异较大。临床研究样品的制备工艺应用于批量生产时,往往会出现药品质量不如研究样品的问题。四是我国的化学药品以仿制药为主,创新性药品研发不足。2017年发布的《中国仿制药蓝皮书》显示,在我国现有药品批准文号中,属于化学药品的有10.7万个,其中95%以上是仿制药。且据业内估计70%以上的国产仿制药药效与原研药存在差距,仿制药存在研究不透彻、质量控制不严格以致药效不足的问题。
| 图表编号 | XD00140053100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.04.01 |
| 作者 | 黄铁苗、徐常建 |
| 绘制单位 | 中共广东省委党校经济学教研部、深圳大学中国经济特区研究中心 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式