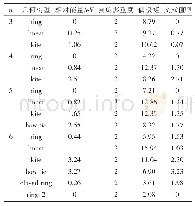
《表2[Mn2+·Ala]构型频率和相应能量》
![《表2[Mn2+·Ala]构型频率和相应能量》](http://bookimg.mtoou.info/tubiao/gif/FDXB202002014_02000.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《密度泛函理论方法研究Mn~(2+)催化丙氨酸反应的机理及催化活性》
C1—O4键旋转涉及到过渡态1-2、4-6L和9-10,自由能垒低于60.6kJ·mol-1;C1—C2键旋转的过渡态是3-4,自由能垒为4.9kJ·mol-1;可知键旋转在常温下容易进行.O4—H8键断裂的过渡态是4-5,自由能垒为7.7kJ·mol-1,可知羧基质子H8容易迁移到氨基上.C2—H7键断裂的过渡态是6L-7,自由能垒只有4.3kJ·mol-1,可见H7从C2迁移到Mn2+上变为平面构型7非常容易;构型7中的H7回迁至C2需要的活化自由能为78.7kJ·mol-1,可知Mn2+催化作用下丙氨酸分子手性转化反应在常温下是动力学允许的.N6—H8键断裂的过渡态是12-13,自由能垒为43.6kJ·mol-1;N6—Mn2+键断裂的过渡态是2-3,自由能垒为119.1kJ·mol-1.C1—C2键断裂的过渡态是1-9,自由能垒为200.3kJ·mol-1;C1—O4键断裂过渡态是10-11,自由能垒为152.8kJ·mol-1;这两个断键反应在动力学上难以在常温下发生.H8在O4和O5两个原子间迁移的过渡态是1-8,自由能垒为171.2kJ·mol-1.构型11失CO反应需要的能量为166.4kJ·mol-1;构型13失H2O反应需要的能量为225.2kJ·mol-1裂解反应较难发生.
| 图表编号 | XD00130853800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.04.01 |
| 作者 | 孟祥军、赵红丽、和芹、王磊、苏月、杨静 |
| 绘制单位 | 唐山师范学院化学系、唐山师范学院化学系、唐山师范学院化学系、唐山师范学院化学系、唐山师范学院化学系、唐山师范学院化学系 |
| 更多格式 | 高清、无水印(增值服务) |



![表2[Mn2+·Ala]构型频率和相应能量](http://bookimg.mtoou.info/tubiao/gif/FDXB202002014_02001.gif)
