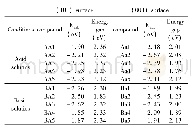
《表1 CO, NO, NO2, SO2, O2和H2S吸附于Cd G最稳定构型的吸附能 (Ea) 、吸附长度 (d) 及基底到各分子的电荷转移 (c)》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《气体分子吸附调控CdG电子结构和磁性的第一性原理研究》
接下来,研究了CO、NO、NO2、SO2、O2和H2S在CdG基底上的吸附行为。建模时,考虑到各气体分子在Cd上不同方向的吸附,根据吸附能的最大值和吸附体系能量最低值,确定了最稳定的吸附结构,如图2所示。通常情况下,当Ea大于0.200 eV,两原子间成键的距离小于0.300 nm,则认为发生化学吸附[32]。表1给出了各吸附构型的吸附能Ea,吸附长度d及电荷转移量c。由吸附能和吸附长度得知,各气体分子与基底均属于化学吸附,同时与Cd原子键合,形成Cd-X键(X表示O、C、N、S原子);较大的电荷转移量表明基底与气体分子间的相互作用很强。另外,每个气体分子吸附对应的最稳定吸附构型与CdG结构相比较,Cd原子与最近C原子之间的高度(hCd-C)增加,气体分子的键长(hd)拉长。例如,对于具有最大吸附能的NO2@CdG结构,吸附NO2分子后,hCd-C和hd分别延伸了8.840%和4.590%。这表明,气体分子的化学吸附可以使它们的结构发生变化。
| 图表编号 | XD0072983800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.06.01 |
| 作者 | 张建宁、马欢、马玲、张建民 |
| 绘制单位 | 宁夏大学物理与电子电气工程学院、宁夏大学物理与电子电气工程学院、宁夏大学物理与电子电气工程学院、陕西师范大学物理学与信息技术学院 |
| 更多格式 | 高清、无水印(增值服务) |
![表1 不同CO*覆盖度下,CO*二聚反应在Cu(100)、Cu(111)和Cu(110)晶面上的吸附能ΔGad、活化能垒ΔEa和反应能ΔE[62]](http://bookimg.mtoou.info/tubiao/gif/KXTB202031008_02300.gif)