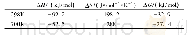《表1 氨分解反应的热力学平衡转化率[40]Tab.1 Thermodynamic equilibrium conversion rate of ammonia decomposition react
氨分解是一个可逆的吸热反应。从表1可以看出,在常压、400℃时,理论上氨基本能完全分解转化。然而实际上氨分解的活化能非常高,有实验证明在常压及不加催化剂的条件下,即使反应温度高达700℃,氨分解的实际转化率也不超过10%[39,40]。而在高温低压条件下,NH3可经催化作用逐步脱氢生成NH2、NH、N,最后两个H和两个N原子分别结合形成H2和N2[41,42]。因此选用合适的催化剂降低反应活化能是促进氨有效分解的核心技术。
| 图表编号 | XD0052523000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.03.18 |
| 作者 | 徐也茗、郑传明、张韫宏 |
| 绘制单位 | 北京理工大学化学与化工学院、北京理工大学化学与化工学院、北京理工大学化学与化工学院 |
| 更多格式 | 高清、无水印(增值服务) |
查看“表1 氨分解反应的热力学平衡转化率[40]Tab.1 Thermodynamic equilibrium conversion rate of ammonia decomposition reaction”的人还看了
-

- 表2 在室温 (298 K) 下团簇Mn3BP各稳定构型转化过程的反应速率常数k和平衡常数K Tab.2 Reaction rate constants (k) and equilibrium constant (K) for change
-
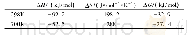
- 表2 不同温度下合成氨反应的热力学参数Tab.2 Thermodynamic parameters of ammonia synthesis at different temperatures N2 (g) +3H2 (g) =2NH3 (
![《表1 氨分解反应的热力学平衡转化率[40]Tab.1 Thermodynamic equilibrium conversion rate of ammonia decomposition react](http://bookimg.mtoou.info/tubiao/gif/HXTB201903004_28500.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式