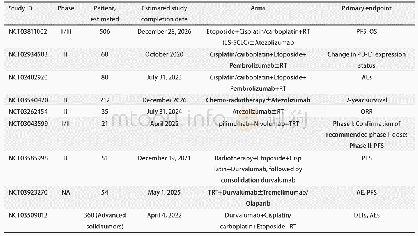
《表1 正在进行的T-Vec临床试验》
资料来源于https://clinicaltrials.gov,截止日期为2018年8月30日
T-Vec治疗肝癌Ⅰ期临床研究纳入对象包括转移性肝癌(A组)和原发性肝癌患者(B组),每组又分为3个剂量组:初始剂量为1×106pfu/ml,随后剂量分别增至1×107pfu/ml(C1)、1×108pfu/ml(C2,≤4 ml)、1×108pfu/ml(C3,≤8 ml),每隔3周注射1次。HECHT等[35]对A组的C1、C2的12例患者进行了安全性评估,认为肝内多针次注射T-Vec治疗转移性肝癌安全可耐受,最高耐受剂量为1×108pfu/ml。现其与PD-1抑制剂联合治疗的研究正在进行中(NCT02509507)。此外,T-Vec治疗软组织肉瘤、乳腺癌等临床试验(表1)正在进行中。
| 图表编号 | XD0048418200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.04.25 |
| 作者 | 姚星妹、潘莉莉、吴婷 |
| 绘制单位 | 厦门大学公共卫生学院分子疫苗学和分子诊断学国家重点实验室国家传染病诊断试剂与疫苗工程技术研究中心、厦门大学公共卫生学院分子疫苗学和分子诊断学国家重点实验室国家传染病诊断试剂与疫苗工程技术研究中心、厦门大学公共卫生学院分子疫苗学和分子诊断学国家重点实验室国家传染病诊断试剂与疫苗工程技术研究中心 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式