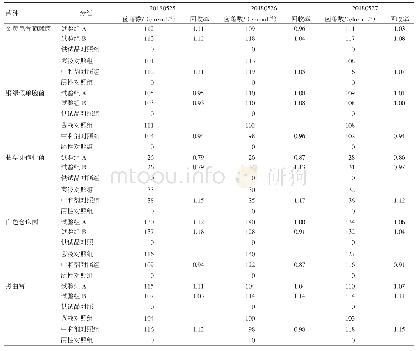
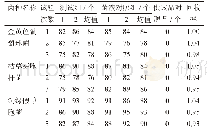
《表1 38批医院制剂需氧菌总数计数 (TAMC) 按剂型分类分布》
41个批次样品的生产日期均为2017年2月之后,微生物限度标准均应符合《中国药典》2015年版四部通则1107的要求。除去3批样品因为制剂生产方(医院K)未提供2015年版《中国药典》方法适用性试验资料,未做检查外,具有有效检查数据的为38批。38批样品按照制剂类型及限度分为口服固体制剂不含药材原粉,口服固体制剂含药材原粉,口服液体制剂及外用制剂。试验结果表明:从表1、图1、表2、图2可以看出,口服固体制剂不含药材原粉类,3批样品均有微生物检出,且需氧菌总数、霉菌和酵母菌总数结果偏高,表明存在一定的微生物污染风险。口服固体含药材原粉类,总体分布比较平均,需氧菌总数计数93%以上都控制在200 cfu·g-1以内,霉菌和酵母菌总数计数86%以上都控制在20 cfu·g-1以内,因这类药品有药材原粉入药,微生物控制难度较大,因此有微生物生长也属于正常现象,虽然药典规定限度较为宽泛,但也需要严格控制。口服液体和外用制剂类,微生物污染情况较好,需氧菌总数计数81%以上都控制在小于10 cfu·g-1·mL-1以内,霉菌和酵母菌总数计数均控制在小于10 cfu·g-1·mL-1以内,外用制剂类多为化学药类,生产工艺与中成药类相比,微生物污染更容易控制一些。
| 图表编号 | XD0047888100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.01.20 |
| 作者 | 张文燕、郭福庆 |
| 绘制单位 | 天津市药品检验研究院、天津市药品检验研究院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式