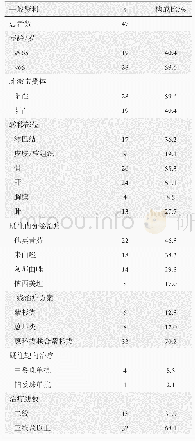
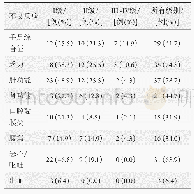
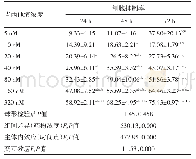
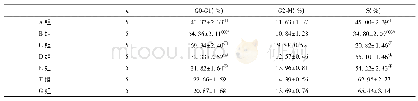
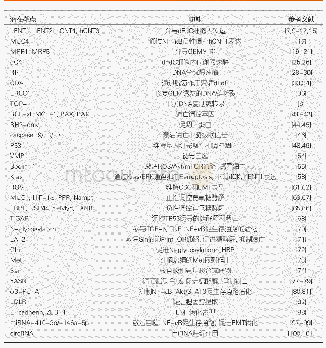
《表1 胰腺癌的细胞内核苷类似物吉西他滨耐药潜在靶点和功能》
hENT:平衡核苷转运体;hCNT:浓缩核苷转运体;MUC:跨膜黏蛋白;MRP:多药耐药相关蛋白;dCK:脱氧胞苷激酶;RR:核糖核酸还原酶;CDA:胞苷脱氨酶;ERCC1:DNA修复内切酶;TOP-I:拓扑异构酶I;BH3-only:唯BH3蛋白;VMP1:自噬相关膜蛋白;Beclin-1:自噬相关基因;Ferroptosis:铁死亡;ROS:活性氧成
胰腺癌是人类最具致命的恶性肿瘤之一,胰腺导管腺癌(pancreatic ductal adenocarcinoma,PDAC)是其中最常见的类型,约占90%.尽管PDAC治疗技术不断进步,但在过去40年中生存率改善有限,其5年生存率仍低于9%,且在所有实体瘤中预后最差[1].目前,手术切除仍是PDAC患者唯一可能治愈的手段,但由于缺乏明确的临床症状或体征使得早期诊断变得异常困难.因此,仅有15%-20%的患者有手术切除的指征[2],对于临界可切除、进展期或转移性PDAC而言,全身化疗(包括新辅助)则是最主要甚或唯一的治疗方案.其中,核苷类似物吉西他滨(gemcitabine,GEM)的单药或联合治疗仍是目前PDAC化疗的一线方案[3].GEM作为一种前药进入PDAC细胞,经过一系列精密调控的磷酸化过程,其衍生物可以干扰DNA合成并阻止癌细胞周期的进展[4](图1).但GEM治疗胰腺癌的总反应率不足20%,约80%的患者可在1年内因肿瘤转移而死亡[5].PDAC对GEM的耐药是影响化疗疗效并导致预后不良的最重要原因之一.因此,克服GEM耐药仍是PDAC治疗中面临的主要挑战之一[6].肿瘤异质性是PDAC耐药性产生的主要原因,其与肿瘤微环境、遗传物质不稳定、细胞内信号分子调控等密切相关,因此GEM耐药机制十分复杂,可能涉及先天性和获得性两个方面,但细胞内信号通路调控是实现GEM抵抗的最终途径(图2).本文将重点讨论GEM在PDAC细胞内的代谢和信号通路调控机制的研究进展(表1).针对这些细胞及分子机制的进一步研究将有助于开发新的化疗增敏策略,提高GEM化疗有效率,改善总体预后.
| 图表编号 | XD00212157500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.11.28 |
| 作者 | 顾宗廷、李宗泽、王成锋 |
| 绘制单位 | 国家癌症中心、国家肿瘤临床医学研究中心、中国医学科学院北京协和医学院肿瘤医院分子肿瘤学国家重点实验室、胰胃外科、国家癌症中心、国家肿瘤临床医学研究中心、中国医学科学院北京协和医学院肿瘤医院分子肿瘤学国家重点实验室、胰胃外科、国家癌症中心、国家肿瘤临床医学研究中心、中国医学科学院北京协和医学院肿瘤医院分子肿瘤学国家重点实验室、胰胃外科 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式