《表1 2,6-二甲氧基苯酚热解初始反应Arrhenius形式动力学参数》
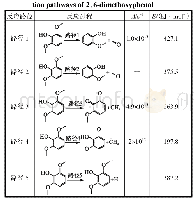
2,6-二甲氧基苯酚在热解过程中的初始路径主要有脱甲氧基、脱甲基和甲氧基重排反应.2,6-二甲氧基苯酚的脱甲氧基过程可以通过协同反应进行,生成2-甲氧基苯酚和甲醛(路径1),该反应的Arrhenius形式的反应速率常数为k=1.0×1013exp(-427.1/RT),见表1.2,6-二甲氧基苯酚的脱甲氧基过程也可以直接通过均裂反应进行(路径2),其反应能垒为375.5 k J/mol.较高的反应能垒表明2,6-二甲氧基苯酚初始过程中直接脱甲氧基反应较难发生.2,6-二甲氧基苯酚的脱甲基过程也可分为协同反应路径(路径3)和自由基均裂反应路径(路径4).其中,路径3的Arrhenius形式的反应速率常数为k=4.9×1013exp(-263.9/RT).而路径4的速率常数为k=2×1015exp(-197.8/RT),其中指前因子2×1015s-1依据苯甲醚热解实验值估算[21].相比较而言,脱甲基的均裂反应更为有利.甲氧基重排起始于2,6-二甲氧基苯酚的自由基脱氢过程,其直接脱氢反应(路径5)的能垒为387.2 k J/mol.由上述结果可知,甲氧基的均裂脱甲基反应是2,6-二甲氧基苯酚的起始热解步骤.
| 图表编号 | XD00205402200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.12.15 |
| 作者 | 戴贡鑫、王冠宇、王凯歌、朱玲君、王树荣 |
| 绘制单位 | 浙江大学能源清洁利用国家重点实验室、浙江大学能源清洁利用国家重点实验室、浙江大学能源清洁利用国家重点实验室、浙江大学能源清洁利用国家重点实验室、浙江大学能源清洁利用国家重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式