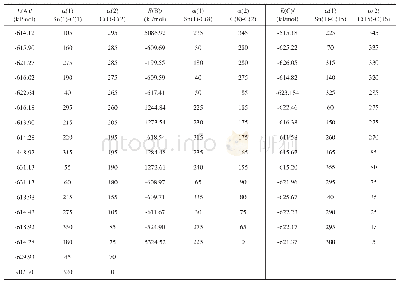
《表4 体系中各配合物的稳定常数》
式中,K′CuY为条件稳定常数,KCuY为稳定常数,αY,αCu为副反应系数。通过以上分析可知:在该浸金体系中,S2O32-和CuY都比较稳定。Cu2+将与EDTA形成1∶1的[Cu(EDTA)]2+,该配合物充当氧化剂,把金氧化成Au+,Au+与S2O32-形成了[Au(S2O3)2]3-,其反应原理如式(4)~(6)所示。从表4可以看出,[Au(S2O3)2]3-比[Cu(EDTA)]2+更稳定,可以使方程式(5)顺利进行。同时[Cu(EDTA)]2+被还原成[Cu(EDTA)]+,空气中的O2又把[Cu(EDTA)]+氧化成[Cu(EDTA)]2+。
| 图表编号 | XD00181682100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.05.01 |
| 作者 | 项朋志、刘龙江、黄遥、叶国华 |
| 绘制单位 | 昆明理工大学国土资源工程学院、云南开放大学化学工程学院、云南开放大学化学工程学院、云南国防工业职业技术学院、云南开放大学化学工程学院、云南国防工业职业技术学院、昆明理工大学国土资源工程学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式