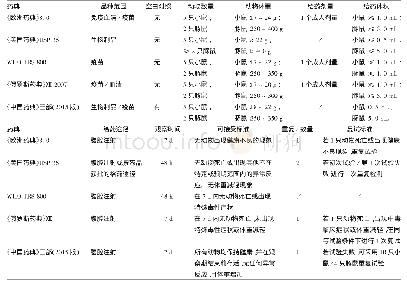
《表1 不同国家药典内生物制品/疫苗异常毒性检测实验条件对比》
注:“/”表示未明确。
在执行异常毒性检测的时期,通过对比各国药典对疫苗产品异常毒性检测的细节要求,发现存在多方面差异[15],见表1。各国对相同疫苗产品的异常毒性检测结果进行相互借鉴的基础欠缺。各国药典在给药剂量、给药体积、观察时间、可接受标准等实际操作规定里存在不同程度的差异。同时各国药典或法规对豚鼠异常毒性检测结果的判定无统一规定或评分标准[4]。可接受标准按严重程度由低到高主要围绕出现特殊毒性体征、观察期内体重减轻、动物死亡3个方面。其中,特殊毒性体征的具体表现定义模糊,对于药典中提到的无异常反应的定性描述,还需结合实际情况进行仔细分辨和判别[16]。出现体征的持续时间长短的判断也未提及,导致不同国家标准涵盖的方面不同,而我国的可接受标准对3个方面同时要求。
| 图表编号 | XD00171483200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.07.20 |
| 作者 | 金苏、姚昕、郭舒杨、项金忠、李敏 |
| 绘制单位 | 国家药品监督管理局药品审评中心、默沙东研发(中国)有限公司、国家药品监督管理局药品审评中心、国家药品监督管理局药品审评中心、国家药品监督管理局药品审评中心 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式