《表2 镁催化的酯硼氢化反应》
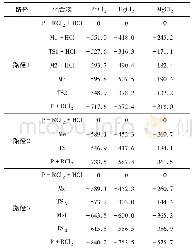
和上述报道的醛酮硼氢化反应相比,酯类化合物由于存在较大的空间位阻和电子效应等因素导致其硼氢化反应相对较难,报道的例子较少.2014年,Sadow等人详细报道了三(4,4-二甲基-2-噁唑啉基)苯基硼酸镁甲基化合物(ToMMgMe,15)催化酯的硼氢化反应[26]室温下,在0.5–5.0 mol%催化量15的作用下,苯或者甲苯为溶剂,一系列酯和2等份HBpin反应6-60分钟,生成相应硼酸酯衍生物(R1CH2OBpin和R2CH2OBpin),产率均达到99%(表2).在上述反应条件下,丙交酯和聚乳酸分别与两等份HBpin反应均得到相应二硼酸酯化合物.然而乙酸乙酯和HBpin在无催化剂的条件下进行反应,即使60°C反应24小时,乙酸乙酯也没有任何转化,这与无催化剂条件下醛与HBpin缓慢反应不同[14].后来证实无催化剂无溶剂条件下,适当提高HBpin与醛的比例至1.4,醛的硼氢化反应在室温或60°C也能很快反应完[27].另外他们还对该反应的机理进行了详细研究,催化剂15可以与酯发生羰基插入反应再通过β-消除得到活性催化剂烷氧基镁化合物16和丙酮副产物,烷氧基镁化合物16再与HBpin反应得到频哪醇硼烷络合镁氢化物和烷基硼酸酯.然而动力学研究显示与传统σ键复分解反应机理不同,他们提出了一种新的两性离子反应机理(图3).烷氧基镁化合物16与酯或从酯可逆分解得到的醛发生反应得到单分子中间体,然后释放出硼氢化产物,同时再生成催化剂烷氧基镁16.
| 图表编号 | XD00161976100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.06.20 |
| 作者 | 罗曼、臧沈荦、姚薇薇、郑晶、马猛涛 |
| 绘制单位 | 南京林业大学理学院化学与材料科学系、南京林业大学理学院化学与材料科学系、南京中医药大学药学院、南京林业大学理学院化学与材料科学系、南京林业大学理学院化学与材料科学系 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式

![表2 氢化反应中贵金属催化剂的性能[37]](http://bookimg.mtoou.info/tubiao/gif/JXHG202006007_03500.gif)
![表4 镁催化的吡啶硼氢化反应[37]](http://bookimg.mtoou.info/tubiao/gif/JBXK202006001_09300.gif)
