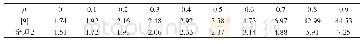《表2 理论计算 (H2O) m (m=1, 2, 3, 7) 助催化H2在Aunδ (n=3~5;δ=0, 1) 上解离的活化能 (△Gact) 和解离反应能 (△Gd) Tab.2 The act
图3对比了不同水簇作用下H2在金簇上的活化能和解离反应能.图3A和C是在中性金簇上(H2O)m助催化H2解离的活化能和解离反应能的变化趋势.除了在Au3上随m值增大而活化能减小外,其它两个簇均随m值增大而增大,且在m=2时出现一个能量转折点,之后再依次减小.在中性金簇上出现能量转折点与水对氢解离机理的影响有关.图3C也表明在热力学上Au4簇最有利于H2解离,其活化能较小.图3B和D分别是带正电簇上活化能和解离反应能的变化.随m值的增大,氢解离反应的自由能显著减小,表明在热力学上H2O显著影响H2解离反应.随(H2O)m簇增大其活化能迅速减小,最后减小为零,这表明水参与H2解离反应,在动力学上极大地促进H2解离反应发生.
| 图表编号 | XD0015003500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2018.06.28 |
| 作者 | 陈家丽、张霞光、吴德印、田中群 |
| 绘制单位 | 厦门大学化学化工学院固体表面物理化学国家重点实验室、厦门大学化学化工学院固体表面物理化学国家重点实验室、厦门大学化学化工学院固体表面物理化学国家重点实验室、厦门大学化学化工学院固体表面物理化学国家重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式