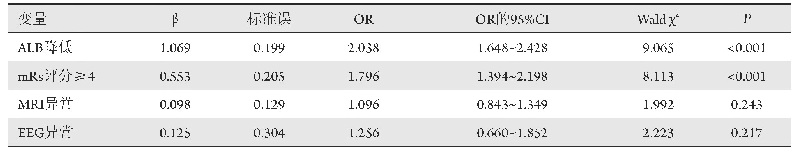
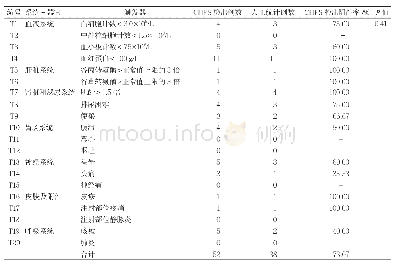
《表2 AE与受试药物的相关性分级》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《盐酸二甲双胍普通片和缓释片在中国健康受试者中的安全性分析》
AE:不良事件(adverse events)
AE是指临床试验受试者接受一种药品后出现的不良医学事件,但并不一定与治疗有因果关系。SAE是指因使用药品引起下述情形之一的反应:(1)导致死亡。(2)危及生命。(3)致癌、致畸、致出生缺陷。(4)导致显著的或永久的人体伤残或器官功能损害。(5)导致住院或住院时间延长。(6)导致其他重要医学事件。AE与受试药物的相关性分为5级:肯定相关、很可能相关、可能相关、可能无关、肯定无关(见表2)。根据CTCAE 4.03标准判断AE严重程度(1~4级)[8]。按照CTCAE 4.03判断标准:频繁的、水样的排便为腹泻,与基线相比大便次数增加,每天<4次判为1级,每天4~6次判为2级,每天≥7次判为3级,危及生命判为4级,死亡判为5级。
| 图表编号 | XD00143325100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.02.29 |
| 作者 | 孙明利、王进、宋秀霞、白海红、刘慧娟、刘晨、佟媛旭、王泽娟、刘晓娜、王瑜、李岩、李银娟、陈刚、李璞、黄俊、王兴河 |
| 绘制单位 | 首都医科大学附属北京世纪坛医院药物Ⅰ期临床试验研究室、首都医科大学附属北京世纪坛医院药物Ⅰ期临床试验研究室、首都医科大学附属北京世纪坛医院内分泌科、首都医科大学附属北京世纪坛医院药物Ⅰ期临床试验研究室、首都医科大学附属北京世纪坛医院药物Ⅰ期临床试验研究室、首都医科大学附属北京世纪坛医院药物Ⅰ期临床试验研究室、首都医科大学附属北京世纪坛医院药物Ⅰ期临床试验研究室、首都医科大学附属北京世纪坛医院药物Ⅰ期临床试验研究室、首都医科大学附属北京世纪坛医院药物Ⅰ期临床试验研究室、首都医科大学附属北京世纪坛医院药物Ⅰ期 |
| 更多格式 | 高清、无水印(增值服务) |