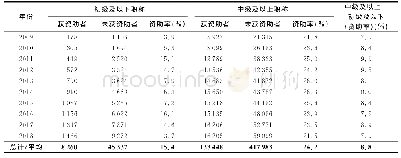
《表1 欧盟CHMP科学建议会议申请费用[5]》
![《表1 欧盟CHMP科学建议会议申请费用[5]》](http://bookimg.mtoou.info/tubiao/gif/YXJZ201912006_01900.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《中国加入ICH为全球新药申报与临床研发带来的机遇与挑战》
欧盟因为有多个成员国,所以申报前沟通会大体上可分为欧盟人用医药产品委员会(CHMP)科学建议会议(scientific advice)或是国家单独申请沟通会议(national scientific advice)。这些会议申请都需要付费,单独的国家沟通会议会比欧盟集中流程的会议申请便宜很多。而且,单独某一个国家的沟通会议流程通常只需要1~2个月,而欧盟流程的会议申请需要3~4个月的时间。但是,单独的欧盟国家的会议讨论结果不一定会形成会议纪要且不具备法律效力,而欧盟的会议则可以得到具备法律效力的会议纪要。表1列出了欧盟CHMP科学建议会议的申请费用。欧盟各个国家申请沟通会议的费用各不相同,但通常会显著低于欧盟CHMP科学建议会议的申请费用。申请欧盟的咨询会议是一项策略性很强的工作,问哪些问题、如何问问题、走欧盟科学建议会议流程还是国家单独申请的沟通会议流程,或者是二者都申请,需要根据产品的具体情况好好规划。因为,一旦开过欧盟科学建议会议,申请国家的单独咨询就会被拒绝。而国家单独咨询除了便宜和快捷外,更重要的是基于欧盟国家药品批准的机制,某一类药物或产品通常会由欧盟内部有限的几个国家的特定审评员主导相关的审评工作。因此,提前通过国家单独咨询的流程接触到这些审评员,了解并影响他们的意见和想法,对于欧盟CHMP科学建议会议以及后续的产品注册上市都会有较大的帮助。
| 图表编号 | XD00141128600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.12.25 |
| 作者 | 张明平、李长青 |
| 绘制单位 | 精鼎医药研究开发(上海)有限公司、精鼎医药研究开发(上海)有限公司 |
| 更多格式 | 高清、无水印(增值服务) |
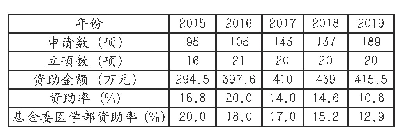
![表2 欧盟药物临床试验质量管理规范(GCP)检查员会议覆盖主题[7,8]](http://bookimg.mtoou.info/tubiao/gif/XYYL202007007_01300.gif)