《表1 Pre-IND会议流程扼要》
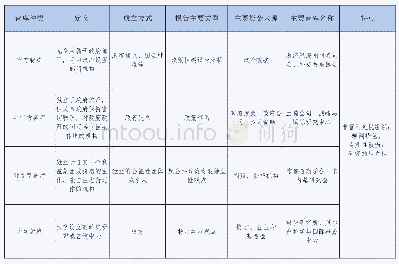
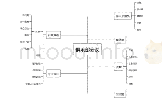
中药、民族药国际化包括临床前研究、临床研究申请、新药上市申请等一系列工作。在申报IND之前,企业与FDA将针对新药注册的相关问题进行PreIND会议,通过该会议积极与FDA进行交流沟通,企业可以获取更多FDA对于药物开发方面的建议,掌握FDA的要求,从而少走弯路和走错路,提高申报成功率。处方药申报者付费法案(Prescription Drug User Fee Act,PDUFA)将FDA与申办方之间的会议分为Type A、Type B、Type B(end of phase,(EOP))、Type C四种类型,Pre-IND会议属于Type B,Pre-IND会议流程见表1[2]。
| 图表编号 | XD00138133900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.12.20 |
| 作者 | 杨洋、周林、谭慧、符德欢、朱兆云、曹国丽 |
| 绘制单位 | 云南省药物研究所、云南白药集团创新研发中心、云南省中药和民族药新药创制企业重点实验室、云南省药物研究所、云南白药集团创新研发中心、云南省中药和民族药新药创制企业重点实验室、云南省药物研究所、云南白药集团创新研发中心、云南省中药和民族药新药创制企业重点实验室、云南省药物研究所、云南白药集团创新研发中心、云南省中药和民族药新药创制企业重点实验室、云南省药物研究所、云南白药集团创新研发中心、云南省中药和民族药新药创制企业重点实验室、云南省药物研究所、云南白药集团创新研发中心、云南省中药和民族药新药创制企业重点实 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式