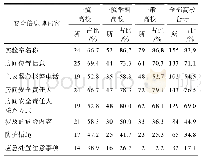
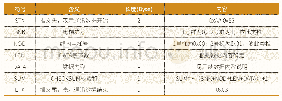
《表3 研究报告应包含的内容》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《创新视角下药品特殊审评与再评价衔接研究——基于欧盟经验》
指南中指出,PASS的研究结果应向公众公开,最好发表于科学期刊。PRAC会对最终研究报告进行评价,并基于研究结果对MAH提出建议。若PRAC建议继续其上市许可,PASS研究即将完成。若PRAC建议更改、暂停或者撤销上市许可,建议会被送至人用药品委员会(the committee for medicinal products for human Use,CHMP),CHMP会对建议进行充分考虑并做出决定,如果决定和PRAC的意见一致,欧盟会根据该意见采取行动。
| 图表编号 | XD00129034900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.12.30 |
| 作者 | 颜建周、张丽杨、雷璐倩、邵蓉 |
| 绘制单位 | 中国药科大学国家药物政策与医药产业经济研究中心、中国药科大学国家药物政策与医药产业经济研究中心、中国药科大学国家药物政策与医药产业经济研究中心、中国药科大学国家药物政策与医药产业经济研究中心 |
| 更多格式 | 高清、无水印(增值服务) |