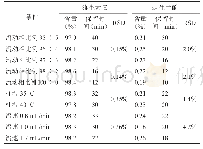
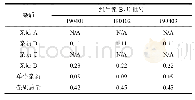
《表6 EMA抗生素有关物质标准制订指导原则中对报告、鉴定和界定的阈值》
对药物杂质谱的控制是保证药品用药安全的重要环节,仿制药一致性评价研究过程中,杂质谱的研究更是与原研制剂质量比对的重要指标。目前上市的氨基糖苷类抗生素均为发酵及半合成来源,与化学合成工艺相比,发酵工艺更具多变性,不易控制,因此与单纯使用化学合成生产的产品相比,生产工艺含有发酵步骤的活性物质的杂质分布一般比较复杂和难以预测,ICH Q3指南不适合用于此类产品的杂质谱研究。2012年6月,EMA(European Medicines Agency)正式发布了抗生素有关物质标准制订指导原则[26],这也是国际上首个针对抗生素杂质研究制订的指导原则。该指南旨在为不适用于ICH Q3指南的发酵产品或源于发酵产品的半合成物质中杂质质量标准的设定提供指导,对于活性成分为发酵或半合成来源的抗生素制剂产品的相关杂质。该指南给出了报告、鉴定和界定阈值,在活性物质由多个密切相关的化合物混合组成(family)情况下,对其应用一般的阈值存在困难。针对此,该指南就如何设定阈值和如何论证杂质谱给出了具体指导(表6),但同时特别强调,该指南不可回顾性使用,即不适用于已完成注册上市销售的产品,但可作为欧洲药典专论修订的重要参考。
| 图表编号 | XD0011681700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.11.25 |
| 作者 | 袁耀佐、张玫、金少鸿 |
| 绘制单位 | 国家药监局化学药品杂质谱研究重点实验室、江苏省食品药品监督检验研究院、国家药监局化学药品杂质谱研究重点实验室、江苏省食品药品监督检验研究院、中国食品药品检定研究院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式