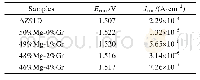
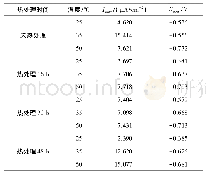
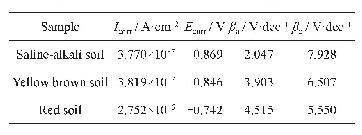《表2 试样的极化曲线参数》
表2为由极化曲线计算出的腐蚀电流密度数据,由表可知,随着溶液温度的升高,腐蚀电流密度升高,在20℃温度下,试样表面的腐蚀电流密度Icorr值最小,仅为0.834μA·cm-2,试样在20℃温度下的耐蚀性最好,在60℃温度下Icorr值最大,为2.836μA·cm-2,试样在60℃下的耐蚀性最差,由此可知,随着溶液温度的升高,试样的耐蚀性能下降,这是由于在中性水溶液中,氧是重要的去极化剂,不锈钢的腐蚀主要是以氧为去极化剂的吸氧反应,同时受扩散控制[5]。一方面,溶液温度升高,Cl-离子的运动速度增大,使得Cl-离子能侵入不锈钢表层的深度增大,另一方面温度升高,氧在水中的溶解氧降低,使得受到破坏的钝化膜不能再次被钝化。氧的溶解量、溶液中离子的运动速度、溶液温度是影响不锈钢表面腐蚀电流密度的主要因素,温度越高,溶解氧含量越低,溶液中离子运动速度越快,试样表层腐蚀电流密度越大,材料的耐蚀性越差。试样在20℃、30℃和40℃溶液中时,H2O和O2容易在氧化膜上吸附,试样的钝化膜完整,当温度升高至60℃时,试样从活化区(曲线bc部分)之后直接进入钝化区,且钝化区间很短,在0.1V左右发生点蚀,温度升高,点蚀电位越低。另外,温度的升高导致的溶解氧含量下降进而降低了钝化膜表面微观区域的pH值,影响钝化膜的稳定性。温度越高,Cl-离子活动能力增强,与表面钝化膜的碰撞几率越大,可以把钝化膜中的氧排挤掉,与钝化膜中的阳离子结合形成可溶性的化合物,诱发点蚀,使钝化膜对机体的保护作用减弱[6]。由此可知,温度对不锈钢表面钝化膜形成有很大的影响,一般而言,钝态不锈钢表面的钝化膜处于不断溶解和修复的平衡状态。在含有Cl-的溶液中,Cl-一般优先吸附在钝化膜上,把氧原子排挤掉,和钝化膜中的阳离子结合成可溶性氯化物,新露出的金属基底则形成点蚀源,进一步发展为点蚀坑,温度的升高提高了Cl-的吸附,使得不锈钢钝化膜的稳定性受到破坏[7-8],材料的耐蚀性急剧下降。
| 图表编号 | XD0085166700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.09.28 |
| 作者 | 杭博、王永霞、魏飞虎、卞小龙、张涛、汪国成 |
| 绘制单位 | 蚌埠学院、蚌埠学院、蚌埠学院、蚌埠学院、蚌埠学院、蚌埠学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式