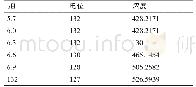
《表1 浸出不同时间的浸出液中Fe/Cu含量比》
图1是分别在p H=3、1和0的硫酸溶液中,温度为110℃,1.0 MPa氧分压条件下,浸出不同时间的黄铜矿电极表面的金相照片。从图1可以看出,黄铜矿在浸出过程中其表面均有不同程度的氧化及钝化现象。新鲜抛光黄铜矿(0 h)表面光滑,呈黄色。当浸出液p H=3时,浸出3 h时的黄铜矿表面生成了致密的赤红色层,随浸出时间延长赤红色层逐渐剥落,剥落后的黄铜矿表面氧化形态稳定。pH=1时,浸出3 h的黄铜矿表面变成氧化色,5 h时表面出现腐蚀小坑且有灰色物产生,10 h时灰色区域扩大但仍可见黄铜矿基底。pH=0时,浸出3 h的黄铜矿表面变成深棕氧化色,5 h时形态模糊,10 h时表面形成了致密的灰色层。从表1不同浸出时间的浸出液中Fe/Cu含量比可以看出,p H=3时,浸出液中的Fe/Cu含量比始终为0;p H值降至1和0时,浸出液中明显有Fe和Cu溶出,Fe/Cu含量比随浸出时间的延长而逐渐减小,且浸出5 h后的Fe/Cu含量比变化很小。从以上结果可知,在pH=3时,随着浸出时间的延长,黄铜矿表面始终存在钝化层,抑制了黄铜矿的氧化,几乎没有金属离子进入溶液。p H值降低(酸度增大),黄铜矿发生氧化分解,且随浸出时间延长表面逐渐形成钝化层,阻碍了黄铜矿的继续氧化浸出。
| 图表编号 | XD0074060600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.05.31 |
| 作者 | 郑永飞、华晓鸣、许茜、鲁雄刚、程红伟、邹星礼 |
| 绘制单位 | 省部共建高品质特殊钢冶金与制备国家重点实验室、上海市钢铁冶金新技术开发应用重点实验室、上海大学材料科学与工程学院、东北大学材料科学与工程学院、省部共建高品质特殊钢冶金与制备国家重点实验室、上海市钢铁冶金新技术开发应用重点实验室、上海大学材料科学与工程学院、省部共建高品质特殊钢冶金与制备国家重点实验室、上海市钢铁冶金新技术开发应用重点实验室、上海大学材料科学与工程学院、省部共建高品质特殊钢冶金与制备国家重点实验室、上海市钢铁冶金新技术开发应用重点实验室、上海大学材料科学与工程学院、省部共建高品质特殊钢冶金与 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式