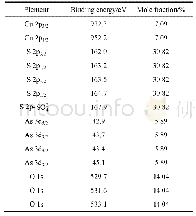
《表4 反应后的-Fe2O3表面铁元素的摩尔分数》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《不同晶型Fe_2O_3催化H_2O_2湿法脱硝的实验研究》
为进一步推测3种Fe2O3催化H2O2分解湿法脱硝的反应机理,实验收集了反应后的?-Fe2O3并进行XPS分析,结果如图12和表4、5所示。对比表1、4可知,与反应前相比,反应后的?-Fe2O3表面的Fe2(10)摩尔分数轻微下降,Fe3(10)摩尔分数有所增加,这说明在反应过程中部分Fe2(10)转换成了Fe3(10)。根据哈伯?韦斯定理(式(4)、(5))[40]可知,Fe2(10)与H2O2的反应速率常数(k1)远大于Fe3(10)与H2O2的反应速率常数(k2),而反应后的?-Fe2O3表面的Fe2(10)和Fe3(10)变化不明显,这种现象表明在催化剂表面部分Fe3(10)被还原成了Fe2(10)。对比表2、5可知,反应后的O?/(O?(10) O?)值下降明显,说明?-Fe2O3表面的氧空位在催化H2O2分解过程中被消耗。因此可以判断,氧空位还原了催化剂表面的Fe3(10)(式(6))。
| 图表编号 | XD00225349100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.10.31 |
| 作者 | 秦阳、潘卫国、郭瑞堂、郭德宇、张中伟、周柒 |
| 绘制单位 | 上海电力大学能源与机械工程学院、上海电力大学能源与机械工程学院、上海发电环保工程技术研究中心、机械工业清洁发电环保技术重点实验室、上海电力大学能源与机械工程学院、上海发电环保工程技术研究中心、机械工业清洁发电环保技术重点实验室、上海电力大学能源与机械工程学院、上海电力大学能源与机械工程学院、上海电力大学能源与机械工程学院 |
| 更多格式 | 高清、无水印(增值服务) |