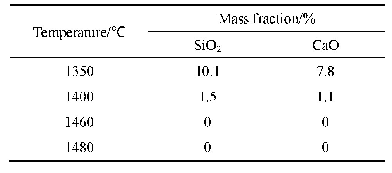
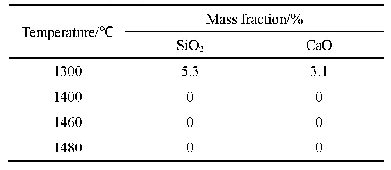
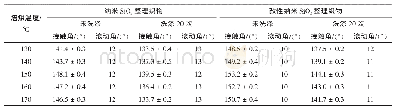
《表1 C8H20O4Si,Si O2,H2O和C2H4的生成焓和各温度下的热力学势》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《流态化气相沉积温度对FeNi_(50)/SiO_2复合粉末形成过程及性能影响》
通过查热力学表[15]可以得出C8H20O4Si,Si O2,H2O和C2H4的生成焓和各温度下的热力学势,结果如表1所示。随后,根据获得的热力学数据,计算出K值预测反应方向和反应程度。图2为在298~1 198 K(25~925℃)温度范围内K值随温度的变化关系。如图2所示,反应平衡常数K随温度的升高而增大,即C8H20O4Si的热分解反应程度逐渐增大。当反应温度低于885.70 K(621.70℃)时K值小于1,表明C8H20O4Si基本不会热分解,当温度大于998 K(725℃)时,C8H20O4Si基本完全热分解。将反应平衡常数K与反应温度的关系用三阶函数进行拟合,拟合结果如式(7)所示。由式(7)可知,只有当反应温度高于885.70 K(621.70℃)时K值才大于1,即有望通过C8H20O4Si的热分解反应,在Fe Ni50合金粉末表面沉积Si O2绝缘层,形成Fe Ni50/Si O2核壳结构。
| 图表编号 | XD00220495100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.10.10 |
| 作者 | 先琛、刘国钊、孔辉、刘莉、方钊、吴朝阳 |
| 绘制单位 | 安徽工业大学冶金工程学院、马鞍山市申马机械制造有限公司、安徽工业大学冶金工程学院、安徽工业大学冶金工程学院、马鞍山市申马机械制造有限公司、安徽工业大学冶金工程学院 |
| 更多格式 | 高清、无水印(增值服务) |