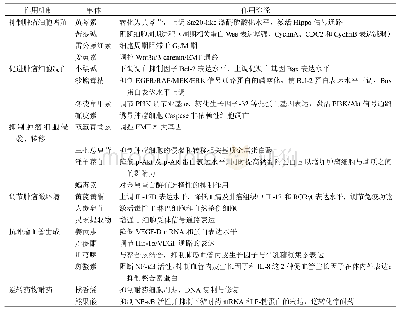
《表1 肿瘤恶病质发病机制》
在肺癌诱导的肿瘤恶病质模型中骨骼肌Toll样受体(TLRs)和髓样分化因子88(MyD88)的基因表达增加。MyD88的靶向消融可抑制肺癌荷瘤小鼠骨骼肌质量和强度的下降,同时MyD88的抑制作用减弱了小鼠骨骼肌中肺癌诱导的未折叠蛋白反应(UPR)激活。此外,X-box结合蛋白1(XBP1)的肌肉特异性缺失可改善肺癌荷瘤小鼠的肌肉浪费,这表明了TLR/MyD88介导的XBP1激活导致肺癌荷瘤小鼠骨骼肌消耗[59]。其他研究也显示,TLRs4的遗传消融和药理学抑制作用都能够减弱带有Lewis肺癌的小鼠恶病质的主要临床标志物,TLR4通过直接激活相关途径(如UPS,自噬溶酶体途径)导致肌管萎缩,增加肌肉分解代谢[60-61]。此外,通过下调肿瘤恶病质小鼠肌肉NF-κB信号通路和肌肉特异性E3泛素连接酶可以有效恢复荷瘤小鼠的骨骼肌功能和质量[26]。有研究表明,通过体内外实验来抑制E3泛素连接酶并激活蛋白激酶B(Akt)/雷帕霉素靶蛋白(mTOR)/转录因子叉头盒O3α(FOXO3α)信号通路可减轻肌肉萎缩并改善成肌细胞分化[62]。综上,不同途径导致肿瘤恶病质作用机制研究归纳见表1。
| 图表编号 | XD00217551800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.01.05 |
| 作者 | 桑亚洲、张艳、刘燕、陈玉龙、吴耀松 |
| 绘制单位 | 河南中医药大学中医药科学研究院河南省中医方证信号传导重点实验室、河南省中医方证信号传导国际联合重点实验室、河南中医药大学中医药科学研究院河南省中医方证信号传导重点实验室、河南省中医方证信号传导国际联合重点实验室、河南中医药大学中医药科学研究院河南省中医方证信号传导重点实验室、河南省中医方证信号传导国际联合重点实验室、河南中医药大学中医药科学研究院河南省中医方证信号传导重点实验室、河南省中医方证信号传导国际联合重点实验室、河南中医药大学中医药科学研究院河南省中医方证信号传导重点实验室、河南省中医方证信号传导 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式