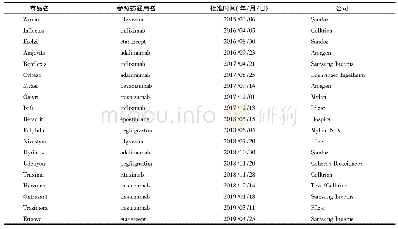
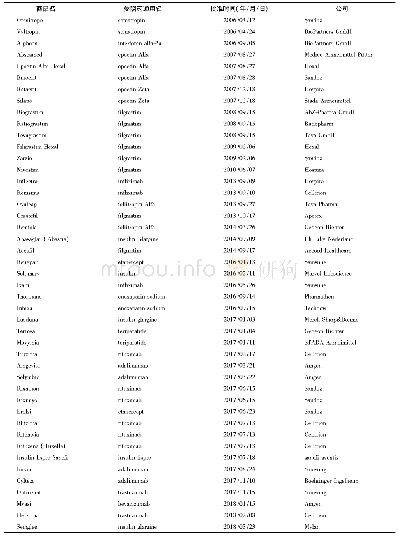
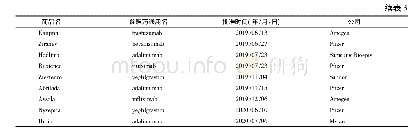
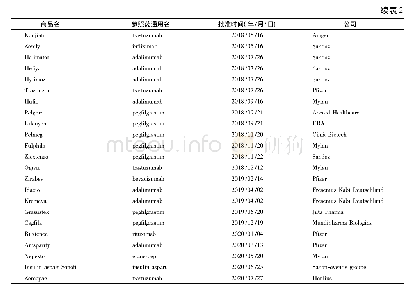
《表4 2020年批准及候选药物批准情况》
ABSSSIs:急性细菌性皮肤及皮肤结构感染;BLA:生物制品许可申请;CKD:慢性肾脏病;GIST:胃肠道间质瘤;LBCL:大B细胞淋巴瘤;MAA:上市许可申请;NDA:新药申请;NMO:视神经脊髓炎;NMOSD:视神经脊髓炎谱系疾病;PDUFA:处方药申报者付费法案来源:Cortellis药物早期研发
EMA正在审查Hansa Biopharma公司的imlifidase的上市许可申请(MAA),该药的适应证为肾移植患者术前的脱敏治疗。Hansa Biopharma于2019年12月22日提交了对第120天问题的回复,审评过程在按计划进行。该公司表示,预计CHMP将于2020年第2季度给出意见,随后欧盟委员会可能于2020年夏季做出决定。有关这些药物和其他2020年预测的概述详见表4。
| 图表编号 | XD00215032800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.12.25 |
| 作者 | Graul AI、Pina P、Tracy M、Sorbera L |
| 绘制单位 | 科睿唯安 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式