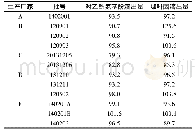
《表1 相似度计算结果:格列美脲片溶出度测定及对其体内外相关性考察》
参考日本医疗用药品质情报集[16]及2015年版中国药典[17]格列美脲片溶出测定法,溶出曲线测定为桨法;转速:50 r·min-1;溶出介质体积900 m L。溶出介质为:(1)水:经脱气纯化水;(2) p H1.2溶出介质的配制:取氯化钠2.0 g与盐酸7 m L,加水并稀释至1 000 m L;(3) p H6.8溶出介质的配制:取磷酸二氢钾3.40 g及无水磷酸氢二钠3.55 g用水溶解并稀释至1 000 m L,用水稀释1倍;(4) p H7.8溶出介质的配制:取磷酸二氢钾0.58 g与磷酸氢二钠22.34 g,加水1 000 m L,振摇使溶解,用10%磷酸溶液或1 mol·L-1氢氧化钠溶液调p H值至7.80。于规定的各时间点取溶出液5 m L(并即补充同温同体积的相应溶出介质)离心,取上清液。按“2.1”项下色谱条件进样,计算累计溶出度,得累积溶出曲线见图1~4,相似度计算结果见表1。结果表明,格列美脲片在不同p H溶出差异大,其中,在p H1.2条件下,溶出度较低,而在p H7.8条件下,溶出过快,故这两种溶出方法无法与体内吸收获得相关,也无法实现控制产品质量的目的。在p H6.8及水条件下,各厂家生产的格列美脲片溶出度曲线区分度大,除A、C及本土化生产的格列美脲片外,其它厂家溶出结果均与原研不相似(f2≥50判定为相似)。
| 图表编号 | XD00213860200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.01.25 |
| 作者 | 叶秀金、陈英 |
| 绘制单位 | 广东省药品检验所、广东省药品检验所 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式