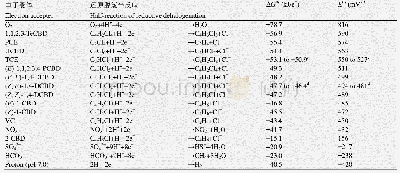
《表1 CO2光还原反应的主要产物及对应的还原电极电势(相对于标准氢电极),p H=7水溶液,25℃[20]》
与传统的、高耗能的捕获或地质封存等手段相比,实现CO2的资源化是一种更具前景的途径,能同时缓解温室效应和能源危机[3-4].基础研究中已开发出热催化[5-7]、光催化[8-10]、电催化[11-13]、光-电协同催化[14-16]和有机催化转化[17-19]等多种途径将CO2分子转化成高附加值的化学品.其中,以太阳能为驱动力的CO2转化(即光催化CO2还原)具备反应条件温和、环境友好等突出优点.光催化CO2还原是模拟自然界植物的光合作用,利用水(H2O)和CO2制造有机物并释放氧气,因此又被称之为“人工光合成”[3,8].热力学上,CO2极其稳定的分子,C=O双键的解离能高达750 k J·mol-1,显著高于还原产物中C—H键(430 k J·mol-1)和C—C键(336k J·mol-1)的键能,这意味着需要向体系注入大量的能量才能触发CO2的活化与转化过程[8].同时,在CO2分子中,碳元素是处于最高的氧化态(+4价),在反应中根据得电子数目的不同可以获得多种产物[8].如表1所示,在光催化反应中,CO2通常可以被还原成一氧化碳(CO)、甲烷(CH4)、甲酸(HCOOH)或乙醇等多种物质,且伴随着水还原生成氢气的副反应,将显著降低目标产物的选择性[20].因此,从目前的研究现状来看,CO2光还原仍旧面临着转化率低和选择性差的困难.为了获得更高的CO2光还原反应效率,催化剂不仅需要有适宜的能带结构,而且需要通过对其表面结构与电子结构进行优化,提高材料对CO2的吸附与活化能力,抑制副产物的生成[8].
| 图表编号 | XD00199769200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.01.15 |
| 作者 | 陈钱、匡勤、谢兆雄 |
| 绘制单位 | 厦门大学化学化工学院、厦门大学化学化工学院、厦门大学化学化工学院 |
| 更多格式 | 高清、无水印(增值服务) |
![《表1 CO2光还原反应的主要产物及对应的还原电极电势(相对于标准氢电极),p H=7水溶液,25℃[20]》](http://bookimg.mtoou.info/tubiao/gif/HXXB202101002_01100.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
![表1 光催化转化CO2反应方程式及相应电极电位表[6]](http://bookimg.mtoou.info/tubiao/gif/ZRZZ202101012_00700.gif)

![表3 铁基MOFs及其衍生物光催化还原CO2的产物[33]](http://bookimg.mtoou.info/tubiao/gif/JXHG202012002_02200.gif)
![表3 计算的[An L]/[An L]–单电子还原反应能以及在THF中的还原电势E0(V,参比电极Fc+/Fc)](http://bookimg.mtoou.info/tubiao/gif/HXXB202010010_03100.gif)