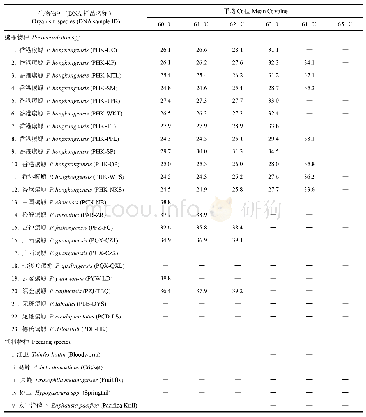
《表1 两种探针吸附不同物种Ig G的解离常数》
本研究合成的聚乙二醇化磁性纳米粒子可特异性结合抗体蛋白,推测是基于砜基的嗜硫作用和聚乙二醇链的抗非特异性吸附功能。其中,嗜硫作用是通过砜基与抗体结构中双硫键的相互作用实现的,因此,不同物种IgG结构的差异可能造成该磁性纳米粒子与抗体蛋白亲和强度的不同。采用BLI传感器测定了人、牛、羊和兔4个物种的IgG在“砜基-聚乙二醇”表面的吸附情况,用以考察此结构的物种选择性,并与Protein A进行比较。BLI传感器是一种基于生物膜干涉技术的实时、无标记生物传感器,生物分子在传感器表面的吸附会引起传感器表面干涉光谱的漂移,漂移程度与传感器表面生物分子的有效吸附量相关,以此实现对生物分子吸附/解离现象的监测[23]。BLI传感器检测的是生物分子动态吸附过程,与静态吸附实验条件不同,结果也会略有不同。图8A为人IgG和BSA在传感器表面的吸附/解离过程,结果表明,“砜基-聚乙二醇”结构对人IgG具有良好的选择性吸附。通过检测不同浓度IgG的吸附/解离过程,得到了IgG在“砜基-聚乙二醇”结构与Protein A传感器探头表面的等温吸附曲线(图8B),计算得到不同物种IgG在两种结构表面的解离平衡常数(表1)。“砜基-聚乙二醇”结构结合IgG具有一定的物种选择性,其与IgG的结合强度为羊>牛>兔>人,这可能是由于不同物种IgG分子中二硫键的数量和位置的不同造成的。需要指出的是,Protein A配基是与抗体的Fc恒定区片段结合,与砜基嗜硫作用的结合的部位有所不同,这可能是两者吸附抗体的物种选择性不同的原因。上述结果表明,“砜基-聚乙二醇”结构结合IgG具有一定的物种选择性,且区别于目前广泛使用的Protein A配基。
| 图表编号 | XD0018754800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2018.12.01 |
| 作者 | 程昉、冯前程、何炜、赵鲜明、汪晴 |
| 绘制单位 | 大连理工大学精细化工国家重点实验室、大连理工大学制药科学与技术学院、大连理工大学制药科学与技术学院、大连理工大学精细化工国家重点实验室、大连理工大学化工学院、大连理工大学制药科学与技术学院、大连理工大学精细化工国家重点实验室、大连理工大学制药科学与技术学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式


![表2 不同Ig G沉积程度的病理损伤比较[M(全距)]](http://bookimg.mtoou.info/tubiao/gif/YXXX202019023_01100.gif)
![表1 不同年龄段患者Ig M和Ig G抗体假阳性结果[n(%)]](http://bookimg.mtoou.info/tubiao/gif/LCJY202008005_01900.gif)