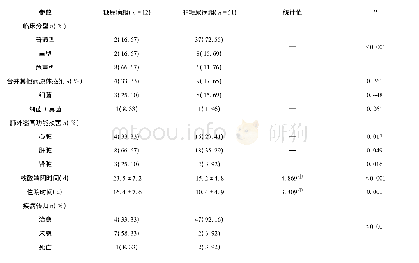
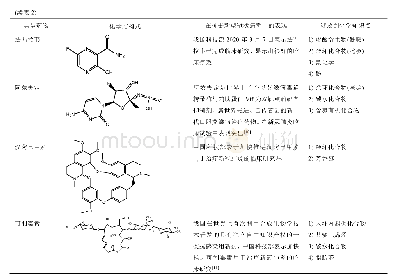
《表1 新冠病毒药物或疗法临床试验项目a)》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《抗击新型冠状病毒肺炎的药物和治疗方案的阶段性研究进展》
a)“临床试验阶段不适用”表示该临床试验不适用于FDA定义的临床试验阶段,包括一些设备试验或行为干涉试验
在中国临床试验注册中心注册的临床试验中,涉及化学药品39个、中药32个、生物制剂21个(由于同一项临床试验可能试验多个药品,所以药品总数多于临床试验项目数).其中,化学药品的临床试验中,涉及氯喹、磷酸氯喹、羟氯喹、硫酸羟氯喹的共有11项临床试验;涉及洛匹那韦/利托那韦的临床试验有10项;阿比多尔或盐酸阿比多尔有3项;ASC09/利托那韦,巴洛沙韦酯、法匹拉韦、甲泼尼龙各有2项;此外还有达芦那韦/考比司他、阿兹夫定、硫辛酸、聚肌胞、甘草酸二铵肠溶胶囊联合维生素C片、芦可替尼等进入临床试验.这些药物中,上市后药物13项,临床处于探索性研究阶段有10项,临床4期阶段有3项.中药临床试验涉及多种中药辨证疗法和中成药及注射剂,其中8项属于上市后药物的疗效确认,其他为探索性研究.生物制剂中,包括间充质干细胞、干扰素、胸腺肽、重组细胞因子基因衍生蛋白、免疫血浆、肠道菌群、脐血单个核细胞、抗衰活性冻干粉、PD-1、托珠单抗、重组病毒巨噬细胞炎性蛋白等制剂单用及与化学药品的联用绝大多数处于探索性研究阶段.
| 图表编号 | XD00165374800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.08.10 |
| 作者 | 邢颖、刘文彬 |
| 绘制单位 | 中国科学院科技战略咨询研究院、中国科学院生态环境研究中心 |
| 更多格式 | 高清、无水印(增值服务) |