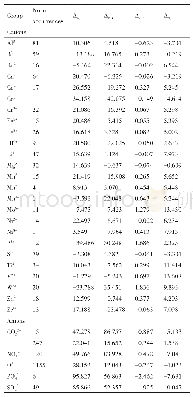
《表1 当氯离子被其他离去基团取代时的活性[17]》
构效关系研究表明,内酯环是Marizomib的关键药效基团,在维持对蛋白酶体抑制活性方面起着至关重要的作用。同时氯乙基也是必要基团[14-16],当氯乙基被未卤代的基团取代会导致Marizomib对20S蛋白酶体的抑制活性降低,而氯离子被其他卤族元素取代时,仍有良好的活性(如碘乙基,IC50=(2.8±0.5)n M;溴乙基,IC50=(2.6±0.4)n M;氟乙基,IC50=(9.2±10.2)n M),这主要是由于其他卤素的离去能力也能形成高度稳定的四氢呋喃环[15]。同时在该位置上的其他离去基团,例如O-Ms(甲基磺酰基,IC50=(4.3±0.8)n M)和O-Ts(甲苯磺酰基,IC50=(2.5±0.4)n M),也产生了等效的抑制活性[16]。同时,C2氯乙基位置的立体化学结构对于活性也很关键[17],与Marizomib相比,氯乙基位置差向异构体活性衰减超过100倍[IC50=(330±20)n M]。环己烯环有利于Marizomib与蛋白酶体结合口袋之间的相互作用,在此位置基团的改变可能会导致效力降低和对蛋白酶体三个蛋白酶解位点的选择性变化。同时大分子烷基如环戊基,环戊-2-烯基和(2S,3R)-环氧环己基取代环己烯基比小分子烷基和芳族取代基取代环己烯基活性更好一些[17]。此外,C3位置甲基和C5位置的羟基是两个不可或缺的抗肿瘤活性基团,当被C3-Et(IC50=(2100±100)n M)或C5-O(酮,IC50=(8200±600)n M)取代导致>1000倍活性降低[17]。活性的降低与仅容纳C3-Me大小蛋白酶体活性位点口袋以及C5-OH与蛋白酶体之间形成氢键密切相关。
| 图表编号 | XD00132483800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.03.01 |
| 作者 | 吉胡瓦、盛华、马宇衡、布仁 |
| 绘制单位 | 內蒙古医科大学、內蒙古医科大学、內蒙古医科大学、內蒙古医科大学 |
| 更多格式 | 高清、无水印(增值服务) |
![《表1 当氯离子被其他离去基团取代时的活性[17]》](http://bookimg.mtoou.info/tubiao/gif/GZHA202005014_01000.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式