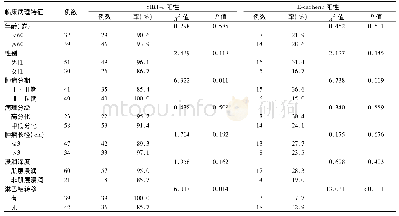
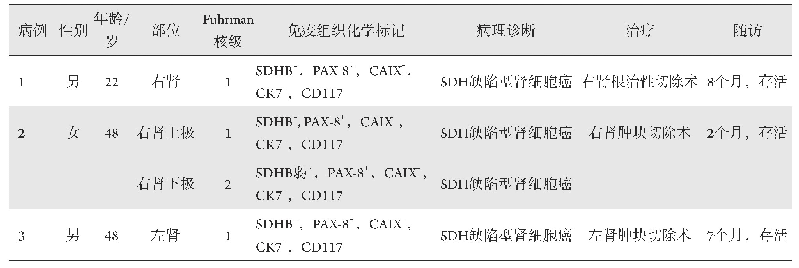
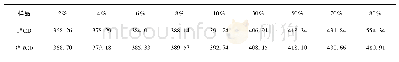《表1 不同RCD的主要细胞生物学特征比较》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《铁死亡信号介导抗肿瘤作用的细胞器调控机制研究进展》
ACSL4:酰基辅酶A合成酶长链家族成员4;ALOX15:花生四烯酸15-脂氧合酶;AURKA:极光激酶A;BAX:BCL2相关蛋白X;BCL2:B细胞淋巴瘤2蛋白;BID:BH3互作域死亡激动蛋白;ESCRT-III:运输所需的内体分选复合物III;GSDMD:穿孔素D(Gasdermin D);HSPA5:热休克蛋白家族A成员5;IL-1β:
铁死亡细胞形态学上主要表现为线粒体变小、嵴减少或消失、膜皱缩和外膜破裂。Dixon等归纳了铁死亡细胞的3个基本特征,即还原性铁的激活、含多不饱和脂肪酸(polyunsaturated fatty acid,PUFA)的磷脂的过氧化、脂质过氧化物修复功能损失[1]。外源因素诱导的铁死亡通路涉及蛋白质(如谷胱甘肽过氧化物酶4,glutathione peroxidase 4,GPX4)、脂质(如PUFA)和氨基酸(如半胱氨酸)等调节因子构成的信号网络的调控。这些特征完全不同于其他RCD,具体独特的生物学特性见表1。铁死亡与自噬存在关联,当细胞响应于铁死亡诱导剂后,自噬小体积聚、细胞内铁贮存蛋白的铁蛋白降解、铁水平上调,促进细胞活性氧(reactive oxygen species,ROS)的积累而引发铁死亡;自噬激活可有利于细胞铁死亡,敲低自噬相关基因可抑制铁死亡;自噬抑制剂氯喹(chloroquine,CQ)也可防止依赖于铁死亡的组织损伤[3]。此外,分子伴侣介导的自噬(chaperonemediated autophagy,CMA)参与铁死亡过程,Erastin诱导CMA分子标志的溶酶体相关膜蛋白2A水平增加可促进GPX4降解,而抑制CMA可稳定GPX4并减少铁死亡[4]。
| 图表编号 | XD00129209500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.03.30 |
| 作者 | 郭倪君、林忠宁、林育纯 |
| 绘制单位 | 分子疫苗学和分子诊断学国家重点实验室厦门大学公共卫生学院、分子疫苗学和分子诊断学国家重点实验室厦门大学公共卫生学院、分子疫苗学和分子诊断学国家重点实验室厦门大学公共卫生学院 |
| 更多格式 | 高清、无水印(增值服务) |