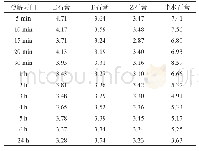
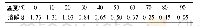《表1 碳酸锂在不同温度水中溶解度》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《基于复杂网络视角下的高纯碳酸锂应用与制备方法研究》
利用碳酸锂溶解度随温度升高逐渐降低的特性,碳酸锂溶解度变化如表1所示。对于不同凝胶的去杂情况,我们选择了Zr(OH)4,Ti(OH)4、凝胶作为去杂剂,进行实验。具体操作为:分别用氯化错和四氯化钦水溶液取代硝酸钵溶液,通常将粗碳酸锂用HCl或H2SO4等无机酸溶解后,经过滤等除杂工序,除去大多数的Ca、Mg等金属杂质离子,在电解反应,锂离子通过隔膜进入阳极溶液,而氢氧根不能通过隔膜进入阳极溶液。由于碳酸锂不溶于水,分解后的碳酸锂会结晶。产率降低,Fe3+以FeO2的形式留在母液中,残留量会有所降低[3]。对于把粗碳酸锂研磨,然后加入水以制备浆料,搅拌,过滤并洗涤,得到碳酸锂浓缩物;通过加入氧化钙过滤粗氢氧化锂溶液进行苛性碱反应过滤。在进行实验中,会产生了大量带负电荷的金属氢氧化物凝胶,并且使用凝胶吸附溶液中的金属杂质来达到净化目的。严格要求提取浓度,提取时间,提取液的p H值等条件。同时,在反应过程中产生大量酸性产物,产生一定的环境压力,从而制备出高纯度的碳酸锂。
| 图表编号 | XD0086491500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.09.11 |
| 作者 | 孙永龙 |
| 绘制单位 | 青海盐湖佛照蓝科锂业股份有限公司 |
| 更多格式 | 高清、无水印(增值服务) |