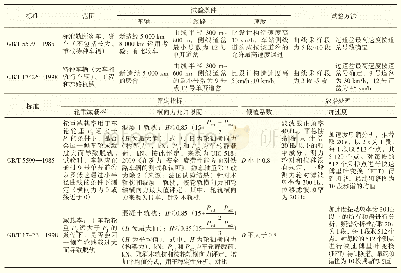
《表3.GB/T16886.5-2017MTT法试验结果》
总之,目前GB/T 16886.5-2017中的MTT法和GB/T14233.2-2005的MTT法作为国家标准,被多数企业直接引用到评价申报医疗器械生物安全性,但是并不代表该试验方法适合所有医疗器械。同时,体外细胞毒性试验条件和临床实际使用的环境条件存在差别,尤其某些降解、溶出的材料应谨慎对待[5]。当前医疗器械产品种类繁多,发展迅速,如何客观的评价医疗器械的细胞毒性,方法的选择尤为重要,需要全面了解产品的理化性质,尽量模拟样品实际使用情况或严于样品实际使用条件进行试验。建议根据产品材料的不同,选择适宜的细胞毒性试验方法。
| 图表编号 | XD0082747000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.05.15 |
| 作者 | 刁立琴、康莉、付钊、高保栓、韩婷 |
| 绘制单位 | 河北省医疗器械与药品包装材料检验研究院、河北省医疗器械与药品包装材料检验研究院、河北省医疗器械与药品包装材料检验研究院、河北省医疗器械与药品包装材料检验研究院、河北省医疗器械与药品包装材料检验研究院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式