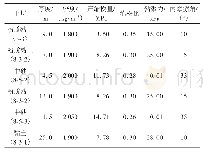
《表1 典型SEs降解、转化酶的主要物理化学性质[28]》
注:aEC编号:酶委员会编号(Enzyme Commission number),bORP:氧化还原电位(Oxidation reduction potential),-为无可利用数据
FEs主要包括雌酮(Estrone,E1)、17α-雌二醇(17α-Estradiol,17α-E2)、17β-雌二醇(17β-Estradiol,17β-E2)、雌三醇(Estriol,E3)。氧化还原酶去除FEs的主要作用机制为氧化耦合反应,催化FEs A环酚羟基形成高氧化潜能、高活性的C2、C4位自由基与C3位苯氧自由基等自由基中间体(图3),通过C-O-C、C-C共价键自耦合、相互耦合形成二聚体,同时受到溶剂类型、pH、A环取代位置等影响[14,18,21,31-32]。FEs A环C3位氧原子的电荷密度较高而自旋密度较低,因此与C-O-C键相比,在动力学上更有利于形成C-C键聚合产物[33]。二聚体可继续形成自由基,作为酶的底物继续氧化耦合生成三聚体、低聚体,甚至高聚体,但聚合物的溶解度随相对分子质量增加急剧降低,难以进一步耦合形成高分子量的聚合物[32,34]。氧化还原酶催化FEs生成的聚合产物溶解度较低,在污水处理过程中易于通过吸附、过滤、沉淀等作用被去除。氧化还原酶的催化能力通常与氧化还原电位(表1)和糖基化程度相关,高氧化还原电位有利于酶对SEs的催化氧化,在一定范围内,酶的稳定性随糖基化程度的增加而提高,其中LiP的糖基化程度较高,为20%-30%,高于HRP(18%-22%)、Lac(10%-20%)和MnP(5%-15%)[35-36]。PODs和Lac催化机理的主要区别在于电子受体,通常PODs以H2O2作为电子受体催化其活性,同时还需要辅酶因子的参与,而Lac以空气或水中的氧分子作为电子受体,不需额外添加氧化剂[17,34,37-39]。FEs在Lac催化体系中的去除速率低于PODs,但PODs不稳定,在复杂基质及过量H2O2条件下易于失活,而Lac的稳定性更强[34]。另外,与A环C3位相结合的CEs(如E1-3S、17β-E2-3S、E1-3G、17β-E2-3G)受到硫酸盐或葡糖苷酸盐基团的保护,不易被氧化还原酶催化氧化形成自由基[22]。不同基质中氧化还原酶对FEs的去除效率如表2所示。
| 图表编号 | XD0041596700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.04.26 |
| 作者 | 余薇薇、杜邦昊、张敏讷、万巧玲、杨硕、赵晨菊 |
| 绘制单位 | 重庆交通大学河海学院水利水运工程教育部重点实验室、重庆交通大学河海学院水利水运工程教育部重点实验室、重庆交通大学河海学院水利水运工程教育部重点实验室、国家城市供水水质监测网重庆监测站、重庆交通大学河海学院水利水运工程教育部重点实验室、重庆交通大学河海学院水利水运工程教育部重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |
![《表1 典型SEs降解、转化酶的主要物理化学性质[28]》](http://bookimg.mtoou.info/tubiao/gif/SWJT201904021_19300.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式

![表4 部分有机酸的化学性质[27-28]](http://bookimg.mtoou.info/tubiao/gif/NMXK202101010_01300.gif)


![表1 现役的典型超高强度合金钢的化学成分[7,10~28]](http://bookimg.mtoou.info/tubiao/gif/JSXB202004010_01000.gif)