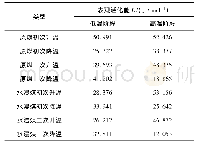
《表1 铁氧化物的速率控制环节与表观活化能的关系》
由此可计算出还原转化率为0.5时的表观活化能E0.5=45.31 kJ·mol-1.同理可求得其他转化率下CF非等温还原的活化能.同样地,H在不同转化率下的还原活化能亦按此求得,结果如图6所示.在相同转化率下,CF的反应活化能均比H大,CF和H的非等温还原平均活化能分别为49.88和43.74 kJ·mol-1;其中,CF第一、第二阶段还原的平均活化能分别为21.13、61.77 kJ·mol-1,H第一、第二和第三阶段还原的平均活化能分别为7.08、16.66和55.82 kJ·mol-1.Nasr等[28]总结前人的研究给出了铁氧化物还原表观活化能与速率控制环节的关系,如表1所示.如图6所示,随着还原度的增加,CF和H的速率控制环节由开始的气体内扩散控制转为气体内扩散与界面化学反应共同控制,最后为界面化学反应控制.总的来看,CF和H还原过程由气体内扩散控制的阶段较为短暂,这是由于样品呈粉末状,孔隙率较大,气体扩散条件优越,有利于CO扩散进入反应界面.
| 图表编号 | XD002838000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2018.11.01 |
| 作者 | 李刚、丁成义、宣森炜、吕学伟、吴珊珊 |
| 绘制单位 | 重庆大学材料科学与工程学院、重庆大学材料科学与工程学院、重庆大学材料科学与工程学院、重庆大学材料科学与工程学院、重庆大学机械传动国家重点实验室、重庆大学材料科学与工程学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式