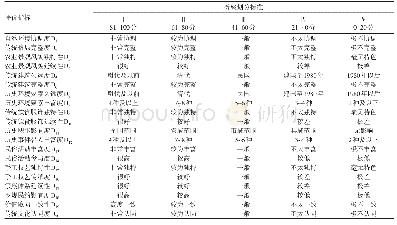
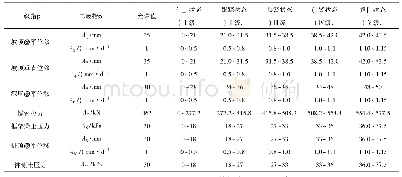
《表2 德国价值评估指标的等级划分标准》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《基于价值定价的多适应证药品医保支付国际经验及启示》
德国卫生部(BMG)规定,2011年后进入德国市场的新药或药品新适应证受德国《医药行业改革法案》(AMNOG)监管,并需强制进行价格谈判[18]。制药企业首先需向联邦委员会(G-BA)提交药品价值评估申请,由G-BA指定药品各适应证的评估对照药品,并要求医疗质量和效率研究所(IQWi G)在收到申请的3个月内审查该药品各适应证的疗效证据,以评估其相较于对照药品的附加治疗效益,并发布评估报告。附加治疗效益一般根据全因死亡率、发病率、健康相关生活质量和不良反应等4个指标为主要判断标准划分为6个等级(具体见表2)[21]。之后,G-BA在评估报告公布的3个月内给出决议,明确该药品的附加治疗效益范围、符合治疗条件的患者群体、以及是否在国家级层面进行药品医保支付全覆盖。
| 图表编号 | XD00216769000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.01.30 |
| 作者 | 代展菁、薛天祺、向贵圆、常峰、路云 |
| 绘制单位 | 中国药科大学国际医药商学院、中国药科大学国际医药商学院、中国药科大学国际医药商学院、中国药科大学国际医药商学院、中国药科大学国际医药商学院 |
| 更多格式 | 高清、无水印(增值服务) |