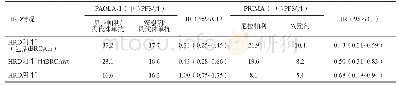
《表4 HRD检测与卵巢癌的铂类药物化疗[44]》
![《表4 HRD检测与卵巢癌的铂类药物化疗[44]》](http://bookimg.mtoou.info/tubiao/gif/ZGAZ202010017_03100.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《上皮性卵巢癌PARP抑制剂相关生物标志物检测的中国专家共识》
目前,全球范围内仅2种HRD检测产品在大型Ⅲ期临床研究中得到验证,并已经得到美国食品药品管理局(Food and Drug Administration,FDA)的批准:Myriad my Choice?CDx(Myriad Genetic Laboratories,Inc.)和Foundation Focus?CDx BRCA LOH(Foundation Medicine,Inc.)。在Myriad My Choice?CDx检测中,HRD阳性定义为肿瘤BRCA1/2突变和(或)GIS评分≥42分,GIS评分由LOH、TAI、LST三项综合计算得出,阈值的设定基于BRCA缺陷的卵巢癌和乳腺癌肿瘤样本第5分位的HRD分值,并最早在乳腺癌和卵巢癌对含铂类药物化疗敏感性的预测中被证实有效(表4)。在Foundation Focus?CDx BRCA LOH检测中,HRD阳性定义为肿瘤BRCA1/2突变和(或)基因组LOH评分≥16%,阈值的设定最初基于其对卵巢癌患者接受含铂类药物化疗效果的有效区分,随后根据其对卵巢癌患者接受rucaparib治疗效果的区分进行了调整[44-46]。
| 图表编号 | XD00215227100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.10.30 |
| 作者 | 温灏、吴焕文 |
| 绘制单位 | 中国医学科学院北京协和医院 |
| 更多格式 | 高清、无水印(增值服务) |