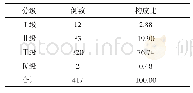
《表1 不良事件分级及描述》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《抗血管生成酪氨酸激酶抑制剂治疗骨与软组织肉瘤的药物安全管理共识》
CTCAE(不良事件通用术语评价标准)最先用于肿瘤临床试验不良事件报告,针对每个不良事件进行严重程度级别划分。最初设计最重要的目的是为了更细致地了解剂量和不良反应之间的关系,它把不良事件(adverse events,AE)的严重程度进行归类,现在广泛使用的是4.03版或者5.0版。肿瘤治疗评估机构(cancer therapy evaluation program,CTEP)发布的CTCAE 5.0从2018年4月1日生效。CTCAE在基于下述的基础原则对每个AE的严重程度(1级~5级)作了特定的临床描述(表1),一般3级以上需要减量或暂停用药。本文将抗血管生成靶向药物比较常见的不良反应处理进行总结。
| 图表编号 | XD00179841300 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.02.28 |
| 作者 | 中国骨肿瘤研究协作组 |
| 绘制单位 | 中国骨肿瘤研究协作组 |
| 更多格式 | 高清、无水印(增值服务) |