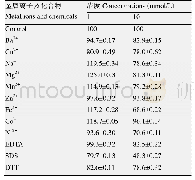
《表2 MaGlu16A纯化表》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《"沙质微泡菌β-1,3(4)-葡聚糖酶的克隆表达及酶学性质"》
注:a:酶活力测定以4%(质量体积比)可得然多糖(curdlan)为底物,在50 mmol/L pH 6.0的柠檬酸冲液体系下,于40°C反应20 min;b:蛋白含量用Lowry法[26]测定,以牛血清蛋白(BSA)为标准.
重组β-1,3(4)-葡聚糖酶(Ma Glu16A)经1 mmol/L IPTG于16°C诱导16 h后,4°C、9 000 r/min离心10 min收集菌体。菌体用缓冲液A重悬后超声破壁,在4°C、12 000 r/min离心10 min即得到粗酶液。粗酶液经Ni-NTA一步纯化得到电泳纯酶,纯化过程中目标蛋白的回收率及纯化倍数见表2,酶活力回收率为54.2%,酶的比活力由26.6 U/mg提高到58.5 U/mg,纯化倍数为2.2(表2)。SDS-PAGE分析在66 kD处显示单一条带,与预测分子量65 kD相近(图3)。
| 图表编号 | XD00174030000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.07.20 |
| 作者 | 马俊文、江正强、李晨霞、闫巧娟 |
| 绘制单位 | 中国农业大学工学院中国轻工业食品生物工程重点实验室、中国农业大学食品科学与营养工程学院、中国农业大学食品科学与营养工程学院、中国农业大学工学院中国轻工业食品生物工程重点实验室 |
| 更多格式 | 高清、无水印(增值服务) |