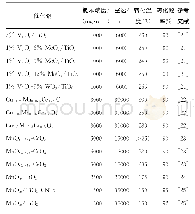
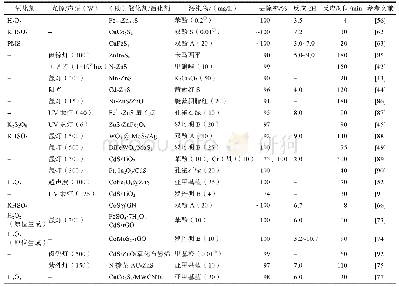
《表1 过渡金属硫化物在高级氧化法中的应用》
(1)mmol/L;(2)s。
反应(1)的速率常数k1=40~80 L/(mol?s),反应(2)的速率常数k2=0.001~0.01 L/(mol?s),反应(3)的速率常数k3=3.3×107 L/(mol?s)。反应(2)是限速步骤,决定了该反应的总速率。即使在催化剂作用下,反应总速率仍然很低,因此,需要大量的H2O2和催化剂Fe2+。另外,由于反应(1)的速率大,而反应(2)的速率小,致使Fe3+过量积累,最终导致均相Fenton反应不仅运行成本过高,还会产生过多的氢氧化铁污泥。此外,反应最适pH范围窄,如表1所示,反应通常在酸性条件下进行。Fenton反应通常在pH=3时效果最好[14-16];当pH升高时,溶液中Fe3+发生水解反应和沉淀,使催化剂催化能力下降,这些缺点限制了Fenton工艺的广泛应用。因此,提高Fe3+还原为Fe2+的速率不仅可以加速污染物的降解,还能减少H2O2的消耗量和铁泥的产生量。
| 图表编号 | XD00163607700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.06.15 |
| 作者 | 王梦哲、陈滢、刘敏 |
| 绘制单位 | 四川大学建筑与环境学院、四川大学建筑与环境学院、四川大学建筑与环境学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式