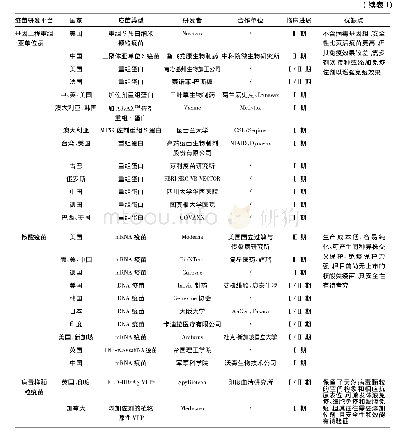
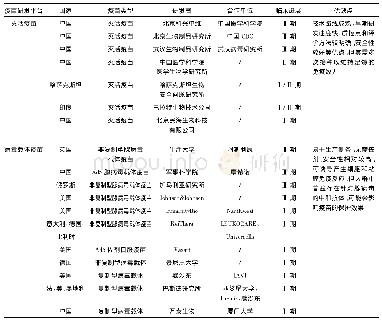
《表2 进入临床试验的腺病毒载体COVID-19疫苗试验设计》
军事医学科学院与康希诺生物股份公司研发的重组腺病毒载体COVID-19疫苗(Ad5-nCoV)以Ad5为载体,将新型冠状病毒(SARS-CoV-2)的刺突(S)蛋白作为靶点,是中国第一个进入临床试验的COVID-19疫苗。I期临床试验于2020年3月16日正式开展,是一项单中心、开放标签、剂量递增的试验,108名志愿者分为高剂量、中剂量和低剂量3组(表2)。根据试验初步结果[46],接种后7d内有87名受试者报告了至少一种不良反应,大多数为轻、中度,但在高剂量更为强烈,主要表现为高热(腋温>38.5℃),伴有疲劳、呼吸困难、肌肉疼痛或关节疼痛,这些不良反应均发生在接种后24h内,持续时间不超过48h且是自限性的。未观察到具有临床意义的实验室指标改变。接种后28d内未发现严重不良事件。接种后14d可诱导产生针对SARS-CoV-2 S-RBD蛋白的特异性抗体(ELISA)以及针对SARS-CoV-2活病毒的中和抗体反应,28d有94%-100%的受试者RBD蛋白特异性抗体滴度(ELISA)比基线水平升高了至少4倍,50%-75%的受试者中和抗体滴度升高了至少4倍,高剂量组抗体反应水平略高于中、低剂量组。该疫苗还在大部分受试者体内诱导产生了快速T细胞应答,并且在高、中剂量组应答更强。此外,高水平的抗Ad5预存免疫会削弱该疫苗的抗体和T细胞应答。
| 图表编号 | XD00159517200 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.08.26 |
| 作者 | 张倩、胡倩倩、王富珍、孙校金、尹遵栋 |
| 绘制单位 | 中国疾病预防控制中心免疫规划中心、中国疾病预防控制中心免疫规划中心、中国疾病预防控制中心免疫规划中心、中国疾病预防控制中心免疫规划中心、中国疾病预防控制中心免疫规划中心 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式


![表2 COVID-19患者呼吸道和消化道病毒核酸持续时间与临床各型之间的关系[中位数(全距)]](http://bookimg.mtoou.info/tubiao/gif/RDYZ202012004_03900.gif)