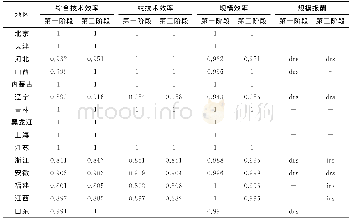
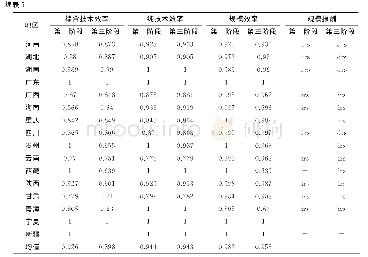
《表1 各离子对的平均第一峰半径和第一配位数》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《LiF-BeF_2熔盐微观结构及扩散特性的分子动力学研究》
①文献[20]的实验测量结果。②文献[17]的分子动力学模拟结果。
图2中绘制了不同温度下LiF-BeF2熔盐中BeF、Li-F和F-F离子对的配位数。可以发现Be-F离子对的配位数随着温度升高而减少,而Li-F和F-F的配位数随温度升高而增加。LiF-BeF2熔盐中各个离子对的平均第一峰半径和配位数如表1所示,可以发现模拟得出的结果与文献[17,20]结果相近。Be-F离子对的平均第一峰半径为1.58?,比Li-F(1.86?)离子对短得多,这也表明Be-F离子对排列的更紧密。从表1可知,Be2+和Li+阳离子的配位数分别为4和4.6,表明Be2+和Li+均可能与F-形成配位数为4的四面体结构。
| 图表编号 | XD00159121300 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.08.01 |
| 作者 | 贺国达、汤睿、段学志、谢雷东、傅杰、戴建兴、钱渊、王建强 |
| 绘制单位 | 中国科学院上海应用物理研究所、中国科学院微观界面物理与探测重点实验室、中国科学院大学、中国科学院上海应用物理研究所、中国科学院微观界面物理与探测重点实验室、华东理工大学化学工程联合国家重点实验室、中国科学院上海应用物理研究所、中国科学院上海应用物理研究所、中国科学院微观界面物理与探测重点实验室、中国科学院上海应用物理研究所、中国科学院上海应用物理研究所、中国科学院微观界面物理与探测重点实验室、中国科学院上海应用物理研究所、中国科学院微观界面物理与探测重点实验室、中国科学院洁净能源创新研究院 |
| 更多格式 | 高清、无水印(增值服务) |