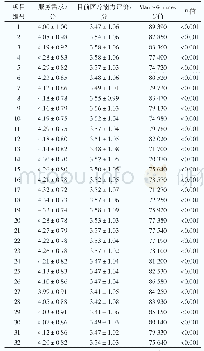
《表3 目前Gla-300的在研项目》
注:GLP-1RA:胰高糖素样肽受体1激动剂;HbA1c,糖化血红蛋白,HEDIS:一种评价有效性的标准(含数据和信息集)
Gla-300已在北美、欧洲、亚洲被批准用于临床。Gla-300在2015年2月25日被美国食品与药品监督管理局(Food and Drug Administration,FDA)批准上市,这主要基于EDITION计划。该项计划是开放标签、随机、平行、26周的一系列研究,其中两个研究额外延长了6个月,评估了Gla-300和Gla-100在1型和2型糖尿病中的疗效、安全性。表2汇总了EDITION计划的设计。本文将回顾与评估Gla-300的药物代谢动力学和药物效应动力学,以及其在临床糖尿病患者中的应用情况,目前进行中的研究(见表3)。
| 图表编号 | XD00127188100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.09.08 |
| 作者 | 谷伟军 |
| 绘制单位 | 中国人民解放军总医院内分泌科 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式