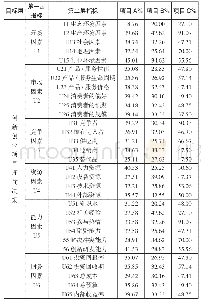
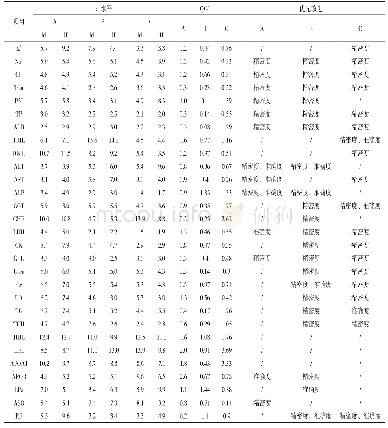
《表1:项目A及项目B执行过程的规范性比较[n (%) ]》
注:同一入组病例会存在多个评价标准的问题,故有总问题例数大于入组例数情况
项目B,入组12例受试者,其中在知情同意书签署环节有3例知情同意书签署时间点存在问题;在项目实施过程中有1例多次出现低血糖情况未采取措施及判断是否属于严重不良反应/事件(SAE),属严重缺陷;在临床试验药物管理方面,发现1例在试验导入期试验药物发放数量不够,有计划外发药情况;在临床试验记录情况方面,10例出现病史未记录或记录不全情况。结果显示,在知情同意书签署情况、临床试验药物管理情况、临床试验记录情况方面,两种随访模式差异无统计学意义(P>0.05),在项目实施过程中方案偏离情况方面,采用全组研究医师共同参与随访模式优于专人随访模式(P<0.05)。见表1。
| 图表编号 | XD0082302900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.05.15 |
| 作者 | 梁锦诗、黄凯文 |
| 绘制单位 | 南方医科大学顺德医院、南方医科大学顺德医院 |
| 更多格式 | 高清、无水印(增值服务) |
![《表1:项目A及项目B执行过程的规范性比较[n (%) ]》](http://bookimg.mtoou.info/tubiao/gif/ZGCF201905033_03100.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式