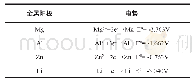
《表3 常见氧化剂在地下水环境中的标准电极电势[8, 15-16]》
![《表3 常见氧化剂在地下水环境中的标准电极电势[8, 15-16]》](http://bookimg.mtoou.info/tubiao/gif/XDDZ201902019_09600.gif) 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《化学氧化技术异位处理地下水非水相有机污染物中试研究》
通过静态实验,分析氧化剂投加量与浊度以及UV254值的关系,确定中试试验氧化剂的投加量或投加范围。UV254值可以代表水中天然存在的腐殖质类大分子有机物以及含CC双键和CO双键的芳香族化合物的相对大小[26]。结果表明,随着氧化剂浓度的增大,UV254值的去除效果增加(图2)。对于高锰酸钾、高铁酸钾、次氯酸钠三种氧化剂,氧化剂浓度成倍增加并未相应地提高去除效果,而是均稳定于40%~55%,说明在2 h内此类氧化剂对地下水的氧化能力已趋近极值。由于地下水pH值偏碱性,电子转移方式的不同可能影响氧化效率[8]。与其他3种氧化剂对比,芬顿试剂对UV254值有较高的氧化效率。Fe2+能够催化H2O2分解产生羟基自由基(·OH),从而引发一系列的链反应,并伴随有铁元素以Fe(Ⅱ)和Fe(Ⅲ)的形式不断相互循环转换[7]。有研究表明,相较于其他氧化剂,芬顿试剂作用于有机污染物的反应更快,对污染物选择性更低、普适性更强[15]。在酸性条件下,芬顿试剂的电极电势可高达2.80 V,远高于常见氧化剂在地下水环境中的标准电极电势(表3)。当H2O2为300 mg/L、Fe2+为150 mg/L、H2O2/Fe2+为2时,在反应进行2 h后,氧化效率可达90%。因此,基于以上结果,选取适宜的氧化剂配比与投加量进行中试研究。
| 图表编号 | XD0044259700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.04.01 |
| 作者 | 盛益之、张旭、翟晓波、李广贺 |
| 绘制单位 | 清华大学环境学院环境模拟与污染控制国家重点联合实验室、清华大学环境学院环境模拟与污染控制国家重点联合实验室、清华大学环境学院环境模拟与污染控制国家重点联合实验室、清华大学环境学院环境模拟与污染控制国家重点联合实验室 |
| 更多格式 | 高清、无水印(增值服务) |

![表1 CO2光还原反应的主要产物及对应的还原电极电势(相对于标准氢电极),p H=7水溶液,25℃[20]](http://bookimg.mtoou.info/tubiao/gif/HXXB202101002_01100.gif)
![表3 酸性介质下标准电极电势[9]](http://bookimg.mtoou.info/tubiao/gif/HXJY202102023_01700.gif)
![表3 计算的[An L]/[An L]–单电子还原反应能以及在THF中的还原电势E0(V,参比电极Fc+/Fc)](http://bookimg.mtoou.info/tubiao/gif/HXXB202010010_03100.gif)