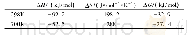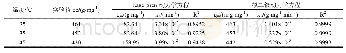《表4 片沸石吸附氨氮的热力学参数Tab.4 Thermodynamic parameters of ammonia adsorption by heulandite》
根据式(9)以及吸附平衡时的吸附量与浓度的比值可得出吉布斯自由能变(ΔG)参数值,见表4。当温度分别为15,25,35,45℃时,得到的ΔG均是负值,表明吸附反应是自发进行的。ΔG绝对值越大,越容易推动反应的进行,再次证实升高温度利于吸附量的增加[19]。结合式(8)对ln(qe/Ce)和1/T进行线性拟合,相关系数为0.994 9。反应的焓变ΔH为12.83kJ/mol。ΔS>0,表明吸附过程中溶液中的氨氮分布杂乱无序。
| 图表编号 | XD0024254300 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2018.02.01 |
| 作者 | 靳薛凯、冯素敏、邵立荣、边永欢、宋振扬、秦晓玲 |
| 绘制单位 | 河北科技大学建筑工程学院、河北科技大学环境科学与工程学院、河北科技大学环境科学与工程学院、河北科技大学环境科学与工程学院、河北科技大学建筑工程学院、河北蓝清水处理科技有限公司 |
| 更多格式 | 高清、无水印(增值服务) |
查看“表4 片沸石吸附氨氮的热力学参数Tab.4 Thermodynamic parameters of ammonia adsorption by heulandite”的人还看了
-
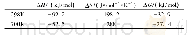
- 表2 不同温度下合成氨反应的热力学参数Tab.2 Thermodynamic parameters of ammonia synthesis at different temperatures N2 (g) +3H2 (g) =2NH3 (
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式