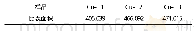《表4 不同方法制备的催化剂的催化性能比较(光照6 min)》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《尖晶石型金属氧化物的制备及光催化有机污染物降解:综述》
Bouchaaba等[79]将Co(NO3)2和Sn O2溶解在硝酸溶液中,采用旋转蒸发的方法除去溶剂并反硝化,最后研磨、焙烧制得尖晶石型CO2Sn O4纳米材料。实验结果表明该材料的禁带宽度为1.7 e V,且该催化剂可吸收可见光的能量。实验证实其在太阳光照射下,对中性红的催化降解率达85%。由于Zn2Sn O4的禁带较宽(3.59 e V),Yan等[80]用化学沉积法将禁带为1.85 e V的BiOI与Zn2Sn O4复合,制得具有异质结构的光催化剂(BiOI/Zn2Sn O4)。他们发现BiOI/Zn2Sn O4既可吸收可见光,亦可吸收紫外光。在光的照射下BiOI/Zn2Sn O4对双酚A、亚甲基蓝和罗丹明B的光催化降解活性大幅提高,明显高于纯BiOI和纯Zn2Sn O4的催化活性。实验结果表明当BiOI的复合量达到35%时,其光催化活性最高,即对亚甲基蓝、双酚A和罗丹明B的催化降解率均接近100%。同时,他们发现BiOI/Zn2Sn O4的结构在反应前后没有改变,表明该催化剂具很有好的稳定性及可重复使用性。机理分析表明(见图8),由于n型Zn2Sn O4的导带电位比p型BiOI的更负,在可见光照射下,只有BiOI能被激发产生电子-空穴。在异质结构的BiOI和Zn2Sn O4内场的影响下,BiOI导带上的光电子被转移到Zn2Sn O4的导带上,而空穴仍保留在BiOI的价带上。但在紫外光照射下,BiOI导带上的光生电子会转移到Zn2Sn O4的导带上,而Zn2Sn O4价带上的空穴又转移到BiOI的价带上,导致光生电子和空穴的有效分离,进而使BiOI/Zn2Sn O4的光催化活性显著提高。并且,光生电子被O2分子捕获产生的·O2-或·OH活性物种可与污染物发生反应;而空穴亦可分解吸附在催化剂表面的污染物或与·O2-反应产生1O2活性物种,1O2又可继续参加降解反应。Yuan等[81]借助微波-水热法制备了Zn Ga2O4纳米粒子。他们为了克服纳米粒子的形状不规则及易发生团聚的问题,采用尿酸作为沉淀剂、十六烷基三甲基溴化铵(CTAB)为表面活性剂,制得高分散、均匀、平均粒度为16.2 nm的纳米粒子,该材料具有70.0 m2/g的比表面积。同时,他们发现加与不加表面活性剂得到的Zn Ga2O4纳米粒子的光催化活性明显不同。对亚甲蓝的光催化实验结果表明,光照18 min,加CTAB制得的Zn Ga2O4纳米粒子催化亚甲蓝的降解率为98%,而不加CTAB制得的Zn Ga2O4纳米粒子催化亚甲蓝的降解率仅为88%。同时,与商业化的光催化剂P25(德固赛公司)及文献[80]报道的Zn Ga2O4纳米粒子的催化性能进行比较(见表4),发现他们制备的Zn Ga2O4纳米粒子的催化活性优于已报道的催化剂的催化性能。
| 图表编号 | XD00146794300 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.08.10 |
| 作者 | 孙宇杰、刘玉芹、徐芬、孙立贤 |
| 绘制单位 | 中国地质大学(北京)材料科学与工程学院、中国地质大学(北京)材料科学与工程学院、桂林电子科技大学材料科学与工程学院广西电子信息材料重点实验室广西新能源材料结构与性能协同创新中心、桂林电子科技大学材料科学与工程学院广西电子信息材料重点实验室广西新能源材料结构与性能协同创新中心 |
| 更多格式 | 高清、无水印(增值服务) |