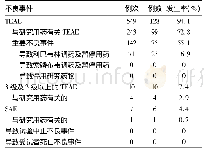
《表2 治疗期不良事件:索磷布韦联合利巴韦林治疗初治基因2型慢性HCV感染者的有效性及安全性分析》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《索磷布韦联合利巴韦林治疗初治基因2型慢性HCV感染者的有效性及安全性分析》
纳入安全性分析的136例受试者中,共有128(94.1%)例受试者报告了549例次治疗期不良事件(treatment emergent adverse event,TEAE),其中与研究用药相关的TEAE 243例次(包括99例受试者,占72.8%)。3级及3级以上的TEAE 10例次(7.4%),其中与研究用药相关的有4例次(2.9%)。重要不良事件共报告142例次(包括75例受试者,占55.1%),其中导致利巴韦林调药或暂停用药的有71例次(包括23例受试者,占16.9%),未出现导致停用研究药物或导致索磷布韦调药或暂停用药的不良事件或重要不良事件。6例(4.4%)受试者发生了7例次SAE,分别为肝低回声区性质待查、早孕后流产、急性上消化道出血、肝内低回声结节、晕厥待查、肝癌,仅1例SAE考虑可能与研究用药有关(肝低回声区性质待查),未出现导致试验中止或受试者死亡的不良事件(表2)。最常见的(发生率≥10%)TEAE包括:血胆红素升高(43.4%)、贫血(27.2%)。
| 图表编号 | XD00120727600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.01.01 |
| 作者 | 宋广军、饶慧瑛、李广明、郭晓林、贾战生、张明香、贾继东、姜相君、郑素军、赵英仁、尚佳、杨兴祥、蔡大川、南月敏、王福生、毛青、谢尧、秦宏、魏来 |
| 绘制单位 | 北京大学人民医院肝病科、北京大学人民医院肝病科、郑州市第六人民医院肝病科、吉林大学第一医院肝胆胰内科、空军军医大学唐都医院传染病肝病中心、沈阳市第六人民医院中西医结合肝病科、首都医科大学附属北京友谊医院肝病中心、青岛市市立医院消化内科、首都医科大学附属北京佑安医院人工肝中心、西安交通大学医学院第一附属医院感染性疾病科、河南省人民医院感染科、四川省人民医院感染科、重庆医科大学附属第二医院感染科、河北医科大学第三医院中西医结合肝病科、解放军总医院第五医学中心肝病生物研究中心、陆军军医大学第一附属医院感染科、首 |
| 更多格式 | 高清、无水印(增值服务) |




![表3 HCV感染或HCV-HIV共感染的无肝硬化或代偿期肝硬化患者[成人(≥18岁)和青少年(12~17岁)],包括初治和经治患者基于基因型的治疗推荐](http://bookimg.mtoou.info/tubiao/gif/LCGD202012012_10200.gif)
